
| |||||||||||||||
 小学生10分钟口算测试100分系列答案
小学生10分钟口算测试100分系列答案科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解

| ||
| ||
| ||
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
![]()
![]()
图2-3-4
(1)写出电解饱和食盐水的化学方程式________________________________________。
(2)已知工艺条件下食盐的溶解度为36.5 g,则该温度下饱和食盐水溶质的质量分数为__________。
(3)设每台电解槽平均每天消耗2.3×104 mol食盐,电解生成的氯气与氢气按体积比1∶1.15通入合成炉,不考虑各阶段的物料损耗,理论上可生产36.5%的盐酸__________t。
(4)氯气与氢气以1∶a(a>1)通入合成炉,设该厂每天消耗食盐c t,不考虑各阶段的物料损耗,则每天生产36.5%的盐酸__________b t。b=__________t。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年重庆市杨家坪中学高二12月月考化学试卷(带解析) 题型:填空题
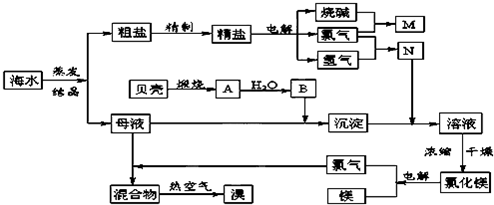
(10分)右面是某化工厂从海水中提取NaCl、Mg(以MgCl2形式存在)和Br2(以NaBr的形式存在)及综合利用的生产流程简图: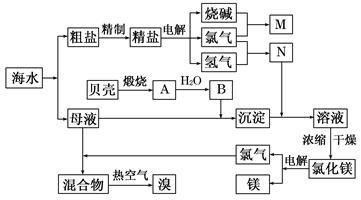
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
A.盐酸 B.氯化钡溶液 C.氢氧化钠溶液 D.碳酸钠溶液。则加入试剂的顺序是(填编号) 。
(2)目前工业上主要采用离子交换膜法电解饱和食盐水,叙述错误的是 。
A.精制饱和食盐水进入阳极室
B.纯水(加少量NaOH)进入阴极室
C.阴极产物为氢氧化钠和氢气
D.电解槽的阳极用金属铁网制成
(3)写出电解饱和NaCl溶液的离子反应方程式: 。
(4)利用MgCl2· 6H2O可制得无水氯化镁,应采取的措施是 。
(5)用热空气吹出的溴蒸气可以用亚硫酸钠溶液吸收,写出反应的化学方程式:
。
查看答案和解析>>
科目:高中化学 来源:2014届重庆市高二12月月考化学试卷(解析版) 题型:填空题
(10分)右面是某化工厂从海水中提取NaCl、Mg(以MgCl2形式存在)和Br2(以NaBr的形式存在)及综合利用的生产流程简图:
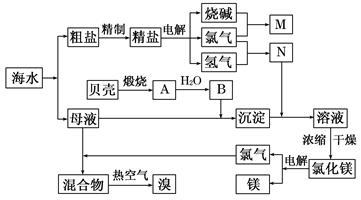
(1)在粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用的试剂为:
A.盐酸 B.氯化钡溶液 C.氢氧化钠溶液 D.碳酸钠溶液。则加入试剂的顺序是(填编号) 。
(2)目前工业上主要采用离子交换膜法电解饱和食盐水,叙述错误的是 。
A.精制饱和食盐水进入阳极室
B.纯水(加少量NaOH)进入阴极室
C.阴极产物为氢氧化钠和氢气
D.电解槽的阳极用金属铁网制成
(3)写出电解饱和NaCl溶液的离子反应方程式: 。
(4)利用MgCl2· 6H2O可制得无水氯化镁,应采取的措施是 。
(5)用热空气吹出的溴蒸气可以用亚硫酸钠溶液吸收,写出反应的化学方程式:
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com