
| A. | 常温下,4.6gNO2和N2O4混合气体中所含原子总数为0.3NA | |
| B. | 4.2g乙烯和丙烯混合气体中含有的极性键数目为0.8NA | |
| C. | 常温下,1L0.5mol/LNH4Cl溶液与2L0.25mol/LNH4Cl溶液所含NH4+的数目相同 | |
| D. | 1mol铁粉在1mol氯气中充分燃烧,转移的电子数为NA |
分析 A、NO2和N2O4的最简式均为NO2;
B、乙烯和丙烯的最简式均为CH2,且CH2中含2条极性键;
C、溶液越稀,盐类水解程度越大;
D、1mol铁在1mol氯气中燃烧时,铁过量.
解答 解:A、NO2和N2O4的最简式均为NO2,故4.6g混合物的物质的量为0.1mol,故含0.3NA个原子,故A正确;
B、乙烯和丙烯的最简式均为CH2,故4.2g混合物含有的CH2的物质的量为0.3mol,且CH2中含2条极性键,故0.3molCH2中含0.6NA条极性键,故B错误;
C、溶液越稀,盐类水解程度越大,故1L0.5mol/LNH4Cl溶液中铵根离子的水解程度比2L0.25mol/LNH4Cl溶液中NH4+的水解程度小,故两溶液中铵根离子的个数不同,故C错误;
D、1mol铁在1mol氯气中燃烧时,铁过量,氯气完全反应,而氯气反应后变为-1价,故1mol氯气转移2NA个电子,故D错误.
故选A.
点评 本题考查了阿伏伽德罗常数的有关计算,难度不大,应注意掌握公式的运用和物质的结构.


科目:高中化学 来源: 题型:选择题
| A. | ①④ | B. | 只有⑥ | C. | 只有⑤ | D. | ④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
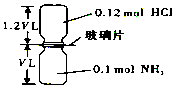 如图,抽去如图所示装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.(已知反应:HCl+NH3═NH4Cl(固体))下列说法正确的是( )
如图,抽去如图所示装置中的玻璃片,使两种气体充分反应(整个过程中认为装置气密性良好),等温度恢复到原来温度.(已知反应:HCl+NH3═NH4Cl(固体))下列说法正确的是( )| A. | 反应后瓶内压强是反应前的$\frac{1}{10}$ | |
| B. | 装置中氢元素的总质量为0.42g | |
| C. | 生成物的分子数目为0.1NA | |
| D. | 反应结束后,两个集气瓶很容易分开 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
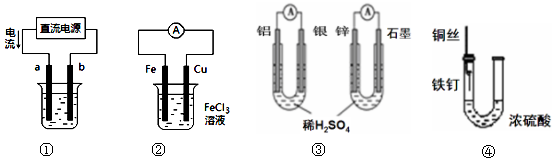
| A. | 用装置①精炼铜,则a极为粗铜,b为精铜,电解质溶液为CuSO4溶液 | |
| B. | 装置②的总反应是:Cu+2Fe3+=Cu2++2Fe2+ | |
| C. | 图③两个装置中通过导线的电子数相同时,消耗负极材料的物质的量不同 | |
| D. | 装置④中的铁钉几乎没被腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 生成 0.1 NA 根共价键 | B. | 消耗反应物总体积 2.24L | ||
| C. | 转移了 2 NA 个电子 | D. | 产物溶于水后,溶液 pH=1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 杜康用高粱酿酒的原理是通过蒸馏法将高粱中的乙醇分离出来 | |
| B. | 蔡伦利用树皮、碎布(麻布)、麻头等原料精制出优质纸张 | |
| C. | 《本草纲目》中记载“(火药)乃焰消(KNO3)、硫磺、杉木炭所合,以为烽燧铳机诸药者”这是利用了KNO3的氧化性 | |
| D. | 英文的“中国”(China)又指“瓷器”,说明我国很早就应用化学技术制作陶瓷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在中和热测定实验中,将碱缓慢倒入酸中,以确保酸碱充分反应 | |
| B. | 为除去蛋白质溶液中混有的(NH4)2SO4,将混合物装入半透膜袋,并放入流动的蒸馏水中 | |
| C. | 用排水集气法收集气体,能验证铜与稀硝酸的反应产物是NO | |
| D. | 向硝酸银溶液中先滴加少量氯化钠溶液,再加少量硫化钾溶液,试管中先有白色沉淀,后有黑色沉淀,则AgCl的溶解度大于Ag2S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
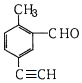
| A. | 能使酸性KMnO4溶液褪色 | |
| B. | 与新制氢氧化铜悬浊液加热煮沸产生砖红色沉淀 | |
| C. | 1mol该物质和H2反应,最多消耗5molH2 | |
| D. | 苯环上的一氯代物有3种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com