
| A. | ①②③④⑤ | B. | ②③④⑥⑧ | C. | ③⑤⑥⑦⑧ | D. | ③④⑤⑥⑧ |
分析 ①硅在自然界中以化合态形式存在;
②SiO2是原子晶体,不存在SiO2分子;
③常见的硅酸盐材料包括玻璃、水泥、陶瓷等;
④二氧化硅为光导纤维主要成分;
⑤氮化硅是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定;
⑥水玻璃是硅酸钠水溶液,是矿物胶,不燃烧,而将硅酸钠涂在木材表面就阻隔了木材与空气中氧气的直接接触;
⑦硅胶具有吸水性,可以作干燥剂干燥一些酸性、中性物质;
⑧氢氟酸能够与玻璃中的二氧化硅反应.
解答 解:①硅元素自然界中以硅酸盐或二氧化硅形式,不存在游离态的硅,故①错误;
②SiO2晶体中每个Si原子与4个O原子成键,每个O原子与2个Si原子成键,晶体中Si原子与O原子数之比为1:2,其化学式为SiO2,SiO2晶体属于原子晶体不存在分子,故②错误;
③水泥是传统硅酸盐产品,其中含有硅酸三钙、硅酸二钙、铝酸三钙,因此普通水泥属于硅酸盐材料,故③正确;
④Si单质是半导体材料,光导纤维的主要成分是二氧化硅,故④错误;
⑤氮化硅陶瓷具有超硬度、耐磨损、抗冷热冲击而不碎裂、耐高温不易传热、抗腐蚀、高温时抗氧化等特性,可用作陶瓷发动机的材料,故⑤正确;
⑥水玻璃是矿物胶,不燃烧,而将硅酸钠涂在木材表面就阻隔了木材与空气中氧气的直接接触,可用作制备木材防火剂的原料,故⑥正确;
⑦硅胶是一种高活性吸附材料,通常是用硅酸钠和硫酸反应,并经老化、酸泡等一系列后处理过程而制得.用于气体干燥、气体吸收、液体脱水等,故⑦正确;
⑧氢氟酸能够与玻璃中的二氧化硅反应,所以能够腐蚀玻璃,可以用来雕刻玻璃,故⑧正确;
故选C.
点评 本题考查硅、二氧化硅及硅酸盐有关知识,明确物质的性质以及用途是解题关键,注意硅与二氧化硅用途的区别,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
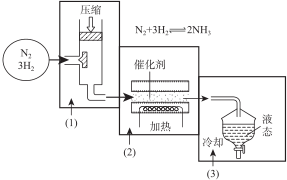
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
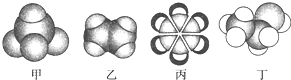
| A. | 甲能使酸性高锰酸钾溶液褪色 | |
| B. | 乙可与溴水发生加成反应使溴水褪色 | |
| C. | 丙中的碳碳键是碳碳单键和碳碳双键交替结合 | |
| D. | 丁不能使酸性高锰酸钾溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去):
A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去):查看答案和解析>>
科目:高中化学 来源: 题型:多选题
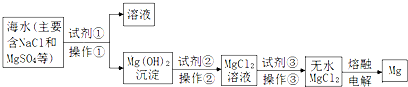
| A. | 试剂①可以选用的试剂是熟石灰,操作①的方法是过滤 | |
| B. | 试剂②可以选用的试剂是盐酸 | |
| C. | 操作③是直接将MgCl2溶液加热蒸发得到无水MgCl2晶体 | |
| D. | 无水MgCl2在通电时发生电离,电解后得到单质Mg. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纸层析法通常以滤纸作为惰性支持物.滤纸纤维上的羟基具有亲水性,它所吸附的水作固定相 | |
| B. | 重结晶时,溶质的溶解度越大、溶液冷却速度越慢,得到的晶体颗粒越小 | |
| C. | 硝酸钾饱和溶液冷却未出现结晶时,可以用玻棒充分磨擦器皿壁促使晶体析出 | |
| D. | 在牙膏的浸泡液中加入新制碱性Cu(OH)2,溶液变绛蓝色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3:2:1 | B. | 1:2:3 | C. | 3:1:1 | D. | 1:3:3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com