
| A. | 0.5mo1H20含有的原子数目为1.5NA | |
| B. | 3.6g石墨和C60的混合物中,含有的碳原子数为0.3NA | |
| C. | 含有4.6g钠元素的过氧化钠和氯化钠的混合物中.所含离子总数为0.3NA | |
| D. | 0.5NA个氯分子的物质的量是0.5mol |
分析 A、水为三原子分子;
B、石墨和C60均由碳原子构成;
C、钠离子的物质的量n=$\frac{4.6g}{23g/mol}$=0.2mol,而无论在氧化钠还是在过氧化钠中,均为2mol钠离子~1mol阴离子,据此分析;
D、根据物质的量n=$\frac{N}{{N}_{A}}$来计算.
解答 解:A、水为三原子分子,故0.5mol水中含1.5mol原子即1.5NA个,故A正确;
B、石墨和C60均由碳原子构成,故3.6g混合物中含有的碳原子的物质的量n=$\frac{3.6g}{12g/mol}$=0.3mol,个数为0.3NA个,故B正确;
C、钠离子的物质的量n=$\frac{4.6g}{23g/mol}$=0.2mol,而在过氧化钠中,2mol钠离子~1mol阴离子,但在氯化钠后,1mol钠离子~1mol阴离子,故当含有0.2mol钠离子时,含有的阴离子介于0.1mol~0.2mol之间,故离子总数介于0.3NA~0.4NA之间,故C错误;
D、物质的量n=$\frac{N}{{N}_{A}}$=$\frac{0.5{N}_{A}}{{N}_{A}}$=0.5mol,故D正确.
故选C.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的使用和物质的结构是解题关键,难度不大.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 氨气在反应中得到电子,表现还原性 | |
| B. | 有1molN2生成时,反应中转移电子数为6NA | |
| C. | 氧化产物与还原产物的质量之比为4:3 | |
| D. | 该反应中各物质均属于非电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Na+、Cl-、NO3- | B. | Mg2+、K+、Cl-、SO42- | ||
| C. | K+、Na+、Cl-、HCO3- | D. | K+、Na+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 28gN2与足量氢气反应,转移电子的数目为6NA | |
| B. | 标准状况下,11.2LHF含有的分子数为0.5NA | |
| C. | 标准状况下,22.4L14CO2与44g14CO2所含分子数均为NA | |
| D. | 2L0.2mol•L-1的稀硝酸与适量铁恰好反应(还原产物只有NO),生成NO的分子数为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 温度 | 250℃ | 300℃ | 350℃ |
| K | 2.041 | 0.270 | 0.012 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 物质名称 | 葡萄糖酸钙 | 葡萄糖酸 | 溴化钙 | 氯化钙 |
| 水中的溶解性 | 可溶于冷水、易溶于热水 | 可溶 | 易溶 | 易溶 |
| 乙醇中的溶解性 | 微溶 | 微溶 | 可溶 | 可溶 |

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 正丁醚(C4H9OC4H9)是惰性溶剂,常用作有机合成反应溶剂.某实验小组利用如图装置(夹持和加热装置均省略)合成正丁醚.发生的反应为:2CH3CH2CH2CH2OH$→_{135℃}^{浓硫酸}$ C4H9OC4H9+H2O
正丁醚(C4H9OC4H9)是惰性溶剂,常用作有机合成反应溶剂.某实验小组利用如图装置(夹持和加热装置均省略)合成正丁醚.发生的反应为:2CH3CH2CH2CH2OH$→_{135℃}^{浓硫酸}$ C4H9OC4H9+H2O| 药品名称 | 性态 | 密度(g/mL) | 熔点(℃) | 沸点(℃) | 水中溶解性 |
| 正丁醇 | 液体 | 0.810 | -89.8 | 118.0 | 微溶 |
| 正丁醚 | 液体 | 0.7689 | -95.3 | 142 | 不溶于水 |
| 备注 | 正丁醇易溶于饱和氯化钙溶液中,而正丁醚微溶 | ||||
查看答案和解析>>
科目:高中化学 来源: 题型:填空题


查看答案和解析>>
科目:高中化学 来源: 题型:选择题
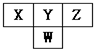 如图是周期表中短周期的一部分.已知Y和W原子能形成两种造成酸雨的有害气体,则下列说法中不正确的是( )
如图是周期表中短周期的一部分.已知Y和W原子能形成两种造成酸雨的有害气体,则下列说法中不正确的是( )| A. | 原子半径的大小顺序是W>Y>Z | |
| B. | X的氢化物没有Z的氢化物稳定 | |
| C. | Z元素的最高价氧化物的水化物的酸性最强 | |
| D. | Y的氢化物比W的氢化物沸点高,是因为分子间存在氢键 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com