
在强碱溶液中,下列各组离子能够大量共存的是
A.Mg2+ 、Ca2+ 、HCO3― 、Cl― B.Na+ 、Al3+ 、ClO― 、SO42―
C.K+ 、Fe2+ 、SO42― 、Br― D.ClO― 、K+ 、Cl― 、SO42―
 高效智能课时作业系列答案
高效智能课时作业系列答案 捷径训练检测卷系列答案
捷径训练检测卷系列答案科目:高中化学 来源:2017届河北省高三上学期一调考试化学试卷(解析版) 题型:选择题
氯气性质的微型实验装置如图所示,①是浓盐酸,⑧是高锰酸钾,②至⑦是滤纸条,依次滴有品红溶液、石蕊试液、淀粉-KI试液、Na2S溶液、KBr溶液、含KSCN的FeCl2几种溶液,实验时挤几滴浓盐酸,下列说法错误的是( )
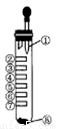
A.产生氯气的离子方程式:16H++ 10Cl-+2MnO4-=2Mn2++5Cl2↑+8H2O
B.⑦处变血红色,是因为2Fe2++Cl2=2Fe3++2Cl-,Fe3++3SCN-=Fe(SCN)3
C.②褪色,③处先变红后褪色,⑤处出现淡黄色固体
D.④处变蓝,⑥处变橙红,能说明氧化性:Cl2>Br2>I2
查看答案和解析>>
科目:高中化学 来源:2017届湖北省松滋市高三上学期9月月考化学试卷(解析版) 题型:计算题
某含氧有机物的相对分子质量为60,1 mol该有机物完全燃烧,生成36gH2O和44.8L CO2(标准状况下)。
(1)求该有机物分子式;
(2)又知此有机物具有弱酸性,能与金属钠反应,也能与碱溶液反应,试写出它可能的结构简式。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省松滋市高三上学期9月月考化学试卷(解析版) 题型:选择题
下列物质中均既有离子键又有共价键的一组是
A.NaOH、H2O、NH4Cl B.KOH、Na2O2、NH4Cl
C.MgO、CaBr2、NaCl D.Na2SO4、HCl、MgCl2
查看答案和解析>>
科目:高中化学 来源:2017届湖北省松滋市高三上学期9月月考化学试卷(解析版) 题型:选择题
下列各组离子中,一定能大量共存的是 ( )
A.加入铝粉只有氢气产生的溶液中:Na+、SO42-、NO3-、Mg2+
B.滴加石蕊试液显红色的溶液中:Fe3+、NH4+、Cl-、SCN-
C.在0.1mol/L的NaHSO4溶液中:NH4+、Na+、Al3+、Cu2+、NO3-
D.在0.1mol/L的NaHCO3溶液中K+、Al3+、Fe3+、NO3-
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省大庆市高三上学期第一次模拟考试化学试卷(解析版) 题型:实验题
某化学兴趣小组制取氯酸钾和氯水并进行有关探究实验。
实验I 制取氯酸钾和氯水
利用下图所示的实验装置进行实验。

(1)盛放浓盐酸的实验仪器名称是 。
(2)A中发生反应的化学方程式是 。
(3)B中生成氯酸钾的离子反应方程式是 。
(4)若对调B和C装置的位置, (填“能”或“不能”)提高B中氯酸钾的产率,原因是 。
实验II 测定圆底烧瓶中反应残余液中盐酸的浓度
圆底烧瓶中所发生的反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学提出下列实验方案:
甲方案:采用酸碱中和滴定法测定。
乙方案:与足量Zn反应,测量生成的H2体积。
继而进行下列实验:
①进行甲方案实验:准确量取冷却后的残余清液,稀释一定的倍数后作为试样。
a.量取试样20.00ml,用0.10mol·L―1NaOH标准溶液滴定,到达滴定终点时,消耗标准溶液24.00ml,则该次滴定所测的试样中盐酸浓度为 ;
b.重复滴定三次后获得实验结果。
②进行乙方案实验:装置如下图所示(夹持器具已略去)。

(i)使Y形管中的残余清液与锌粒反应的正确操作是将 转移到 中,否则会造成实验结果偏低。
(ii)反应完毕,读取H2的体积,读数时应注意:A.冷却至室温b. C.视线与凹液面最低处相切。
查看答案和解析>>
科目:高中化学 来源:2017届黑龙江省大庆市高三上学期第一次模拟考试化学试卷(解析版) 题型:选择题
一定量的混合气体在密闭容器中发生如下反应:xA(g)+yB(g) zC(g),达到平衡后测得A气体的浓度为0.5 mol·L-1,保持温度不变,将密闭容器的容积压缩为原来的一半再次达到平衡后,测得A浓度为0.8 mol·L-1,则下列叙述正确的是( )
zC(g),达到平衡后测得A气体的浓度为0.5 mol·L-1,保持温度不变,将密闭容器的容积压缩为原来的一半再次达到平衡后,测得A浓度为0.8 mol·L-1,则下列叙述正确的是( )
A.平衡向正反应方向移动 B.x+y<z
C.B的物质的量浓度减小 D.C的体积分数降低
查看答案和解析>>
科目:高中化学 来源:2017届西藏日喀则区第一高级中学高三上第一次月考化学卷(解析版) 题型:实验题
(1)某同学欲称量NaOH的质量,他先用托盘天平称量烧杯的质量,天平平衡后的状态如下图所示。烧杯的实际质量为 g,要完成本实验该同学应称出 g NaOH。
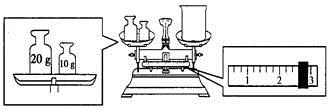
(2)使用容量瓶前必须进行的一步操作是 。
(3)在配制过程中,其他操作都是正确的,下列操作会引起配制浓度偏高的是 。
A.转移溶液时不慎有少量洒到容量瓶外面 |
B.定容时俯视刻度线 |
C.未冷却到室温就将溶液转移到容量瓶并定容 |
D.定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线 |
查看答案和解析>>
科目:高中化学 来源:2017届湖南省高三上学期9月月考化学试卷(解析版) 题型:选择题
A配制FeCl3(aq):称取一定质量的FeCl3(s),加水溶解,再加入稀盐酸酸化
B钠与水的反应:取绿豆大小的金属钠放入烧杯,再滴入两滴酚酞试液,最后加入水
C析出溶质晶体:接近饱和的热溶液,冷却速度越慢得到的晶体颗粒越大
D实验室制氢气:为了加快反应速率,向稀H2SO4中滴加少量Cu(NO3)2(aq)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com