
根据下表(部分短周期元素的原子半径及主要化合价)信息,判断以下叙述正确的是
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.186 | 0.143 | 0.089 | 0.102 | 0.074 |
| 主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
科目:高中化学 来源: 题型:单选题
四种短周期元素在周期表中的位置如图,其中只有M为金属元素。下列有关说法正确的是( )
| A.离子半径Z < M < X |
| B.Y的最高价氧化物对应水化物的酸性比X 的强 |
| C.X 的最简单气态氢化物的热稳定性比Z的大 |
| D.单质沸点:M > X > Y |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下表所示为部分短周期元素的原子半径及主要化合价,根据表中信息判断下列叙述正确的是
| 元素代号 | A | B | C | D | E | F | G |
| 原子半径/nm | 0.152 | 0.160 | 0.089 | 0.143 | 0.102 | 0.099 | 0.071 |
| 主要化合价 | +1 | +2 | +2 | +3 | +6、-2 | -1 | -1 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
X、Y、Z、W是元素周期表中前四周期原予序数依次增火的四种元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子核外只有三个能级,且各能级电子数相等 |
| Y | Y的基态原子最外层电子数是其内层电子总数的3倍 |
| Z | Z的基态原子价电于排布为nsn-1 |
| W | W的单质是一种常见的红色金属,在潮湿的空气中易生成绿色的锈斑 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知X、Y、Z、L四种元素是组成蛋白质的基础元素且原子序数依次增大。回答下列问题:
(1)L的元素符号为________ ;Y元素原子核外电子中,未成对电子数与成对电子数之比为______;四种元素的原子半径从大到小的顺序是____________________(用元素符号表示)。
(2)Z、X两元素按原子数目比l∶3可构成分子A,A的电子式为________;B分子也由Z、X两元素组成,作为运送飞船的火箭燃料,常温下是一种液态化合物。已知该化合物的相对分子质量为32,其中X元素的质量分数为12.5 %,且该分子结构中只有单键。则B的结构式为____________。若64 g B分子与液态双氧水恰好完全反应,产生两种无毒又不污染环境的气态物质,还放出3000 kJ的热量,写出该反应的热化学方程式 。
(3)硒(Se)是人体必需的微量元素,与元素L同一主族,该族第2 ~5周期元素单质分别与H2反应生成l mol气态氢化物产生的热量数据如下,其中能表示生成1 mol硒化氢所产生的热量的是__________(选填字母编号)。
a.—99.7 kJ b.—29.7 kJ c.+20.6 kJ d.+241.8 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
很多国家已停止使用含铊的杀虫剂。元素周期表中铊的数据见右图,下列说法正确的是
| A.TI元素是一种主族元素 |
| B.TI元素的相对原子质量是204 |
| C.铊元素的质量数是204.4 |
| D.TI原子最外层有3个能量相同的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
A、B、C、D是原子序数依次增大的四种短周期元素,甲、乙、丙、丁、戊是由其中的两种或 三种元素组成的化合物,辛是由C元素形成的单质。已知:甲+乙=丁 +辛,甲+ 丙=戊+辛;常温下0.1 mol/L 丁溶液的pH为13。下列说法正确的是
A.元素B在周期表中的位置为第二周期第VIA族
B.元素B、C、D的原子半径由大到小的顺序为r (D) > r(C) > r(B)
C.1.0 L0. 1 mol/L戊溶液中阴离子总的物质的量小于0. 1 mol
D.1 mol甲与足量的乙完全反应共转移了约6.02 X 1023个电子
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列说法错误的是
| A.H2O2和Na2O2都属于氧化物,两种物质中所含的化学键类型完全相同 |
| B.原子核外在离核较远区域的电子易失去,其原因是这些电子能量较高 |
| C.第三周期非金属元素形成氢化物的稳定性从左到右逐渐增强 |
| D.在周期表的金属元素和非金属元素的交界处寻找半导体,在过渡元素区中寻找催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列叙述与对应图式正确的是
A.由下列短周期元素性质的数据推断元素③最高价氧化物对应的水化物碱性最强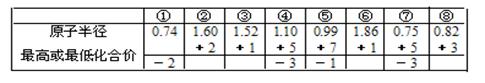 |
B.图甲表示Zn-Cu原电池反应过程中的电流强度的变化,T时可能加入了H2O2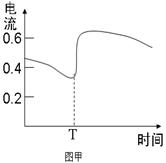  |
| C.图乙表示某一放热反应,若使用催化剂E1、E2、ΔH都会发生改变 |
| D.表示H2燃烧热的热化学方程式为:2H2(g)+O2(g)=2H2O(l);△H= -571.6kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com