


科目:高中化学 来源: 题型:
| A、常温下,1L pH=1的硫酸溶液中含有的H+为0.1NA |
| B、常温下,14g C2H4和C3H6的混合气体中含有2NA个氢原子 |
| C、2.3g Na和足量的O2完全反应,在常温和燃烧时,转移电子数均为0.1NA |
| D、1mol甲醇中含有C-H键的数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 ;
;| 浓H2SO4 |
| △ |
| CH3OH |
| 浓H2SO4,△ |

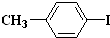 和
和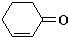 也可以发生类似反应①的反应,有机产物的结构简式为
也可以发生类似反应①的反应,有机产物的结构简式为查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
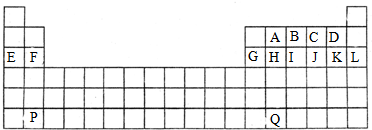
| 1 |
| 2 |
| A、当它可以形成①时,不可能形成④,因为①中R为奇数,④中R为偶数 |
| B、当它可以形成①时,不可能形成②和③,因为偶数族主要为偶数化合价 |
| C、当它可以形成②时,可以形成③和④,且③和④两种离子不能和H+大量共存 |
| D、当它形成②时,也可以形成①,因为①中R元素比②中R元素化合价低 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、合成洗涤剂和纯碱溶液都可洗去衣服上的油污,二者去污原理相同 |
| B、乙醇、天然气、液化石油气、氢气都可以作为燃料电池的原料,其中氢气是最为环保的原料 |
| C、“地沟油”虽然对人体有害,但对“地沟油”进行分馏可制得汽油、煤油,达到变废为宝的目的 |
| D、医药中常用酒精来消毒,是因为酒精能够使细菌蛋白发生变性 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com