
| A. | SO2可以漂白纸浆和草帽辫 | |
| B. | 单质硅可用做半导体材料 | |
| C. | 小苏打可作食品的膨松剂 | |
| D. | 合成纤维和光导纤维都是新型无机非金属材料 |
分析 A.二氧化硫具有漂白性;
B.硅处于金属与非金属交界的元素可以作半导体材料;
C.碳酸氢钠不稳定受热分解生成气体;
D.合成纤维是有机非金属材料,光导纤维是新型无机非金属材料.
解答 解:A.二氧化硫具有漂白性,可以用来漂白纸浆和草帽辫,故A正确;
B.硅处于金属与非金属交界处,所以硅既有金属性又有非金属性,可用做半导体,故B正确;
C.碳酸氢钠不稳定受热分解生成气体,在制作食品时加碳酸氢钠会使食品疏松多孔,故C正确;
D.合成纤维是有机非金属材料,光导纤维是新型无机非金属材料,故D错误;
故选D.
点评 本题考查了二氧化硫、硅、碳酸氢钠性质的应用,高分子化合物的判断,注意知识的积累,题目较简单.


科目:高中化学 来源: 题型:实验题
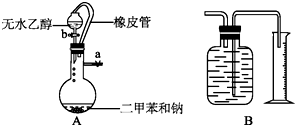 为了测定乙醇的结构式,有人设计了无水酒精与钠反应的实验装置和测定氢气体积的测量装置.
为了测定乙醇的结构式,有人设计了无水酒精与钠反应的实验装置和测定氢气体积的测量装置.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | pH>7,且c(Na +)>c(OH -)>c(H +)>c(CH3COO-) | |
| B. | pH>7,且c(Na +)+c(H+)=c(CH3COO -)+c(OH-) | |
| C. | PH<7,且c(CH3COO -)>c(H+)>c(Na+)>c(OH-) | |
| D. | pH=7,且c(CH3COO -)=c(Na+)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
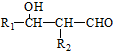
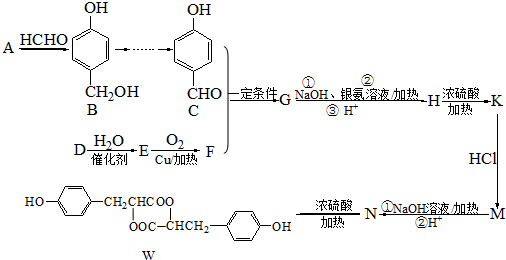
 .
.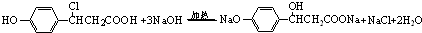 .
.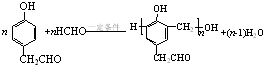 .
.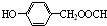 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
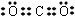 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 操作 | 现象 | 结论 |
| A | 某溶液加入K3[Fe(CN)6]溶液 | 黑色沉淀生成 | 证明原溶液中存在Fe2+ |
| B | 某溶液加入HNO3、BaCl2混合液 | 产生白色沉淀 | 该溶液一定含有SO42- |
| C | 将水蒸气通过灼热的铁粉 | 粉末无变化 | 铁与水蒸汽高温下不反应 |
| D | 将一小块Na放入无水乙醇中 | 产生气泡 | Na能置换出醇羟基中的氢 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高一上第一次月考化学卷(解析版) 题型:推断题
现有三种可溶物质A、B、C,其中A、B是盐,一种是酸式盐,一种是正盐,C是碱,它们溶于水后电离产生的所用离子如下表所示:
阳离子 |
|
阴离子 |
|
请根据下列叙述回答问题:
(1)C的化学式为_________________。
(2)A溶液与B溶液反应可生成气体X,则X的化学式为_______________________, 该反应的离子方程式为___________________.
该反应的离子方程式为___________________.
(3)A、B溶液与C溶液反应可分别生成白色沉淀D和E,其中D可溶于稀硝酸.
①B的化学式为____________,鉴别溶液中B的阴离子的方法是____________________.
②D溶于稀硝酸的离子方程式为________________________.
查看答案和解析>>
科目:高中化学 来源:2016-2017学年安徽省高一上第一次月考化学卷(解析版) 题型:选择题
某同学在实验报告中记录下列数据或操作,其中正确的是
A.用100mL量筒量取8.6mL浓硫酸 B.用托盘天平称量8.75g食盐
C.用500mL的容量瓶来配制需要的450mL溶液 D.用胶头滴管取5mL的某溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com