
”¾»Æѧ”Ŗ”ŖŃ”ŠŽ5£ŗÓŠ»ś»Æѧ»ł“””æ£Ø15·Ö£©
ĻĀĶ¼ÖŠXŹĒŅ»ÖÖ¾ßÓŠĖ®¹ūĻćĪ¶µÄŗĻ³ÉĻćĮĻ£¬AŹĒÖ±Į“ÓŠ»śĪļ£¬EÓėFeCl3ČÜŅŗ×÷ÓĆĻŌ×ĻÉ«”£
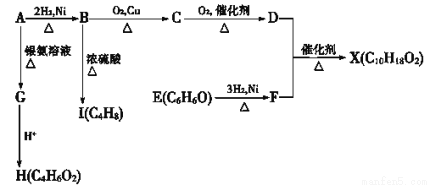
Ēėøł¾ŻÉĻŹöŠÅĻ¢»Ų“š£ŗ
£Ø1£©CµÄĆū³ĘŹĒ__________”£B”śIµÄ·“Ó¦ĄąŠĶĪŖ_________”£
£Ø2£©Ö»ÓĆŅ»ÖÖŹŌ¼Į¼ų±šD”¢E”¢H£¬øĆŹŌ¼ĮŹĒ___________”£
£Ø3£©HÓėJ»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬JŌŚĖįŠŌĢõ¼žĻĀĖ®½āÓŠŅŅĖįÉś³É£¬JµÄ½į¹¹¼ņŹ½ĪŖ___________”£
£Ø4£©ŗĖ“Ź²ÕńĒāĘ×Ķ¼ÖŠDÓŠ_______×é·åĒŅ·åĆ껿֮±ČĪŖ _____________”£
£Ø5£©DŗĶF·“Ӧɜ³ÉXµÄ»Æѧ·½³ĢŹ½ĪŖ_____________________________”£
£Ø1£©¶”Č©£»(2·Ö) ĻūČ„·“Ó¦(2·Ö)£»£Ø2£©äåĖ®(2·Ö)£»£Ø3£©CH3COOCH=CH2(2·Ö)
£Ø4£©4; (2·Ö) 3:2:2:1(2·Ö)
£Ø5£©(3·Ö)
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗE EÓėFeCl3ČÜŅŗ×÷ÓĆĻŌ×ĻÉ«£¬Ö¤Ć÷ŗ¬ÓŠ·ÓōĒ»ł£¬ŹĒ±½·Ó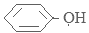 £»EÓėĒāĘų·¢Éś¼Ó³É·“Ó¦²śÉśF£ŗ»·¼ŗ“¼
£»EÓėĒāĘų·¢Éś¼Ó³É·“Ó¦²śÉśF£ŗ»·¼ŗ“¼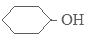 £¬AŹĒÖ±Į¬½į¹¹£¬·¢ÉśŅ»ĻµĮŠ·“Ó¦²śÉśµÄDÓėF·“Ó¦µĆµ½X:C10H18O2£¬XŹĒŅ»ÖÖ¾ßÓŠĖ®¹ūĻćĪ¶µÄŗĻ³ÉĻćĮĻ£¬XŹĒõ„£¬ŌņDŹĒ¶”ĖįCH3CH2CH2COOH;C“ß»ÆŃõ»ÆµĆµ½¶”Ėį£¬ŌņCŹĒ¶”Č©CH3CH2CH2CHO;BŹĒ¶”“¼CH3CH2CH2 CH2OH£»ÓÉÓŚAÄܹ»ÓėŅų°±ČÜŅŗ·¢ÉśŅų¾µ·“Ó¦£¬ŌņAÖŠŗ¬ÓŠČ©»ł£¬1molµÄAÄܹ»Óė2molµÄĒāĘų·¢Éś¼Ó³É·“Ó¦£¬ŌņAÖŠ»¹ŗ¬ÓŠŅ»øöĢ¼Ģ¼Ė«¼ü”£ŌņAæÉÄÜŹĒCH2=CH-CH2CHO,»ņŹĒCH3CH=CHCHO”£GŌņæÉÄÜŹĒCH2=CH-CH2COONH4,»ņŹĒCH3CH=CHCOO NH4”£GĖį»ÆµĆµ½HæÉÄÜŹĒCH2=CH-CH2COOH»ņCH3CH=CHCOOH;ÓÉÓŚBŹĒ¶”“¼£¬ĖłŅŌB·¢ÉśĻūČ„·“Ó¦²śÉśI£ŗ¶”Ļ©CH3CH2CH=CH2”££Ø1£©CµÄĆū³ĘŹĒ¶”Č©£»B”śIµÄ·“Ó¦ĄąŠĶĪŖĻūČ„·“Ó¦£»£Ø2£©DŹĒ¶”Ėį£¬Ö»ŗ¬ōČ»ł£¬ EŹĒ±½·Óŗ¬ÓŠ·ÓōĒ»ł£»HŹĒ¶”Ļ©Ėį£¬ŗ¬ÓŠĢ¼Ģ¼Ė«¼üŗĶōČ»ł£¬ČōÖ»ÓĆŅ»ÖÖŹŌ¼Į¼ų±šĖüĆĒ£¬ŌņøĆŹŌ¼ĮŹĒäåĖ®£¬ÓėäåĖ®·¢Éś·“Ó¦²śÉś°×É«³ĮµķµÄŹĒ±½·Ó£¬Äܹ»ŹĒäåĖ®ĶŹÉ«µÄŹĒ¶”Ļ©Ėį£¬ĪŽČĪŗĪĻÖĻóµÄµÄ¶”Ėį”££Ø3£©H¶”Ļ©ĖįÓėJ»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬JŌŚĖįŠŌĢõ¼žĻĀĖ®½āÓŠŅŅĖįÉś³É£¬ŌņJŹĒõ„£¬ŹĒŅŅĖįŅŅĻ©õ„£¬½į¹¹¼ņŹ½ĪŖCH3COOCH=CH2£»£Ø4£©ŌŚ¶”Ėį·Ö×ÓCH3CH2CH2COOHÖŠŗ¬ÓŠĖÄÖÖ²»Ķ¬µÄHŌ×Ó£¬ĖłŅŌŗĖ“Ź²ÕńĒāĘ×Ķ¼ÖŠDÓŠ4×é·åĒŅ·åĆ껿֮±Č,3£ŗ2£ŗ2£ŗ1£¬£Ø5£©DŗĶF·“Ӧɜ³ÉXµÄ»Æѧ·½³ĢŹ½ĪŖ
£¬AŹĒÖ±Į¬½į¹¹£¬·¢ÉśŅ»ĻµĮŠ·“Ó¦²śÉśµÄDÓėF·“Ó¦µĆµ½X:C10H18O2£¬XŹĒŅ»ÖÖ¾ßÓŠĖ®¹ūĻćĪ¶µÄŗĻ³ÉĻćĮĻ£¬XŹĒõ„£¬ŌņDŹĒ¶”ĖįCH3CH2CH2COOH;C“ß»ÆŃõ»ÆµĆµ½¶”Ėį£¬ŌņCŹĒ¶”Č©CH3CH2CH2CHO;BŹĒ¶”“¼CH3CH2CH2 CH2OH£»ÓÉÓŚAÄܹ»ÓėŅų°±ČÜŅŗ·¢ÉśŅų¾µ·“Ó¦£¬ŌņAÖŠŗ¬ÓŠČ©»ł£¬1molµÄAÄܹ»Óė2molµÄĒāĘų·¢Éś¼Ó³É·“Ó¦£¬ŌņAÖŠ»¹ŗ¬ÓŠŅ»øöĢ¼Ģ¼Ė«¼ü”£ŌņAæÉÄÜŹĒCH2=CH-CH2CHO,»ņŹĒCH3CH=CHCHO”£GŌņæÉÄÜŹĒCH2=CH-CH2COONH4,»ņŹĒCH3CH=CHCOO NH4”£GĖį»ÆµĆµ½HæÉÄÜŹĒCH2=CH-CH2COOH»ņCH3CH=CHCOOH;ÓÉÓŚBŹĒ¶”“¼£¬ĖłŅŌB·¢ÉśĻūČ„·“Ó¦²śÉśI£ŗ¶”Ļ©CH3CH2CH=CH2”££Ø1£©CµÄĆū³ĘŹĒ¶”Č©£»B”śIµÄ·“Ó¦ĄąŠĶĪŖĻūČ„·“Ó¦£»£Ø2£©DŹĒ¶”Ėį£¬Ö»ŗ¬ōČ»ł£¬ EŹĒ±½·Óŗ¬ÓŠ·ÓōĒ»ł£»HŹĒ¶”Ļ©Ėį£¬ŗ¬ÓŠĢ¼Ģ¼Ė«¼üŗĶōČ»ł£¬ČōÖ»ÓĆŅ»ÖÖŹŌ¼Į¼ų±šĖüĆĒ£¬ŌņøĆŹŌ¼ĮŹĒäåĖ®£¬ÓėäåĖ®·¢Éś·“Ó¦²śÉś°×É«³ĮµķµÄŹĒ±½·Ó£¬Äܹ»ŹĒäåĖ®ĶŹÉ«µÄŹĒ¶”Ļ©Ėį£¬ĪŽČĪŗĪĻÖĻóµÄµÄ¶”Ėį”££Ø3£©H¶”Ļ©ĖįÓėJ»„ĪŖĶ¬·ÖŅģ¹¹Ģ壬JŌŚĖįŠŌĢõ¼žĻĀĖ®½āÓŠŅŅĖįÉś³É£¬ŌņJŹĒõ„£¬ŹĒŅŅĖįŅŅĻ©õ„£¬½į¹¹¼ņŹ½ĪŖCH3COOCH=CH2£»£Ø4£©ŌŚ¶”Ėį·Ö×ÓCH3CH2CH2COOHÖŠŗ¬ÓŠĖÄÖÖ²»Ķ¬µÄHŌ×Ó£¬ĖłŅŌŗĖ“Ź²ÕńĒāĘ×Ķ¼ÖŠDÓŠ4×é·åĒŅ·åĆ껿֮±Č,3£ŗ2£ŗ2£ŗ1£¬£Ø5£©DŗĶF·“Ӧɜ³ÉXµÄ»Æѧ·½³ĢŹ½ĪŖ ”£
ӣ
æ¼µć£ŗæ¼²éÓŠ»śĪļµÄ½į¹¹”¢ŠŌÖŹ”¢×Ŗ»Æ”¢·“Ó¦ĄąŠĶµÄÅŠ¶Ļ”¢»Æѧ·½³ĢŹ½ŗĶĶ¬·ÖŅģ¹¹ĢåµÄŹéŠ“µÄÖŖŹ¶”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ°²»ÕŹ”øßČżµŚŅ»“ĪĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
¹żŃõ»Æ¼ŲÓėĖ®µÄ·“Ó¦ĄąĖĘÓŚ¹żŃõ»ÆÄĘÓėĖ®µÄ·“Ó¦£¬Ęä»Æѧ·½³ĢŹ½ĪŖ£ŗ
2K2O2£«2H2O=4KOH£«O2”ü
µ±0.5mol K218O2Óė×ćĮæH2OĶźČ«·“Ó¦ŗó£¬ĻĀ±ķ¶ŌÉś³ÉĪļO2µÄŠšŹöÖŠ“ķĪóµÄŹĒ£Ø £©
| K218O2µÄÖŹĮæ | O2µÄŠšŹö |
A | 57g | O2µÄÖŹĮæĪŖ9g |
B | 57g | Éś³É±ź×¼×“æöĻĀO2µÄĢå»żĪŖ5.6L |
C | 114g | O2µÄĦ¶ūÖŹĮæŹĒ32g”¤mol-1 |
D | 57g | Éś³É0.25molO2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģ°²»ÕŹ”½»“Ź®Š£øßČż11ŌĀĮŖæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
»ÆѧÓėÉś²ś”¢Éś»īĆÜĒŠĻą¹Ų,ĻĀĮŠŠšŹö“ķĪóµÄŹĒ
A£®“Óŗ£“ųÖŠĢįČ”µāµ„ÖŹµÄ¹ż³ĢÉę¼°Ńõ»Æ»¹Ō·“Ó¦
B£®øß“æ¶ČµÄ¶žŃõ»Æ¹č¹ć·ŗÓĆÓŚÖĘ×÷¹āµ¼ĻĖĪ¬£¬¹āµ¼ĻĖĪ¬ÓöĒæ¼ī»į”°¶ĻĀ·”±
C£®ĄūÓĆĢ«ŃōÄܵČĒå½ąÄÜŌ““śĢę»ÆŹÆČ¼ĮĻ,ÓŠĄūÓŚ½ŚŌ¼×ŹŌ“”¢±£»¤»·¾³
D£®ĀĢÉ«»ÆѧµÄŗĖŠÄŹĒÓ¦ÓĆ»ÆѧŌĄķ¶Ō»·¾³ĪŪČ¾½ųŠŠÖĪĄķ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģÄžĻÄŅų“ØŹŠøßČżÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠ½āŹĶŹĀŹµµÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ
A£®ĢśŗĶĻ”ĻõĖį·“Ó¦ÖʵĆĒ³ĀĢÉ«ČÜŅŗ£ŗFe + 4H+ + NO3£ £½Fe3+ + NO”ü+ 2H2O
B£®ĮņĖįŃĒĢśČÜŅŗÖŠ¼ÓČėÓĆĮņĖįĖį»ÆµÄ¹żŃõ»ÆĒāČÜŅŗ£ŗ Fe +2H
+2H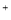 +H2O2=Fe
+H2O2=Fe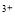 +2H2O
+2H2O
C£®ĻņĖįŠŌKMnO4ČÜŅŗÖŠĶØČėSO2£ŗ2MnO4£+5SO2+4OH££½2Mn2++5SO42£+2H2O
D£®0.01 mol”¤L”Ŗ1 NH4Al(SO4)2ČÜŅŗÓė0.02 mol”¤L”Ŗ1 Ba(OH)2ČÜŅŗµČĢå»ż»ģŗĻ£ŗNH4++Al3++2SO42-+2Ba2++4OH”Ŗ=2BaSO4”ż+Al(OH)3”ż+NH3”¤H2O
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģÄžĻÄŅų“ØŹŠøßČżÉĻŃ§ĘŚĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ŃĪŹĒŅ»Ąą³£¼ūµÄĪļÖŹ£¬ĻĀĮŠĪļÖŹĶعżŅ»¶Ø·“Ó¦æÉÖ±½ÓŠĪ³ÉŃĪµÄŹĒ
¢Ł½šŹōµ„ÖŹ ¢Ś¼īŠŌŃõ»ÆĪļ ¢Ū¼ī ¢Ü·Ē½šŹōµ„ÖŹ ¢ŻĖįŠŌŃõ»ÆĪļ ¢ŽĖį
A£®¢Ł¢Ś¢Ū B£®¢Ł¢Ü¢Ž C£®¢Ś¢Ż¢Ž D£®Č«²æ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģÄžĻÄøßȿ𼶵Ś¶ž“ĪŌĀæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
(13·Ö)Čż·ś»ÆµŖ(NF3)ŹĒŅ»ÖÖĪŽÉ«£¬ĪŽĪ¶µÄĘųĢ壬ĖüŹĒĪ¢µē×Ó¹¤Ņµ¼¼ŹõµÄ¹Ų¼üŌĮĻÖ®Ņ»£¬Čż·ś»ÆµŖŌŚ³±ŹŖµÄæÕĘųÖŠÓėĖ®ÕōĘųÄÜ·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬Ęä·“Ó¦µÄ²śĪļÓŠ£ŗHF”¢NOŗĶHNO3£¬Ēėøł¾ŻŅŖĒó»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©·“Ó¦¹ż³ĢÖŠ£¬±»Ńõ»ÆÓė±»»¹ŌµÄŌŖĖŲŌ×ÓµÄĪļÖŹµÄĮæÖ®±ČĪŖ__________£®
£Ø2£©Š“³öøĆ·“Ó¦µÄ»Æѧ·½³ĢŹ½____________________________________________£®
Čō·“Ó¦ÖŠÉś³É0.2 mol HNO3£¬×ŖŅʵĵē×ÓŹżÄæĪŖ________øö£®
£Ø3£© Čż·ś»ÆµŖæÉÓÉ°±ĘųŗĶ·śĘų·“Ó¦µĆµ½£ŗ4NH3+3F2=NF3+3NH4F ,¾ŻĢāŅāĶĘ²ā NF3”¢F2”¢NOČżÖÖĘųĢåÖŠ£¬Ńõ»ÆŠŌÓÉČõµ½ĒæµÄĖ³ŠņĪŖ____________________
£Ø4£©NF3ŹĒŅ»ÖÖĪŽÉ«”¢ĪŽ³ōµÄĘųĢ壬µ«Ņ»µ©NF3ŌŚæÕĘųÖŠŠ¹Ā©£¬»¹ŹĒŅ×ÓŚ·¢ĻÖ£®ÄćÅŠ¶ĻøĆĘųĢ効Ā©Ź±µÄĻÖĻóŹĒ___________________________________________________.
£Ø5£©Ņ»µ©NF3Š¹Ā©£¬æÉŅŌÓĆNaOHČÜŅŗÅēĮܵķ½·Ø¼õÉŁĪŪČ¾£¬Ęä²śĪļ³żNaNO2”¢NaF”¢H2OĶā£¬»¹æĻ¶ØÓŠ____________________________(Ģī»ÆѧŹ½)£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģÄžĻÄøßȿ𼶵Ś¶ž“ĪŌĀæ¼Ąķ×Ū»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠĪļÖŹ·ÖĄąÕżČ·µÄŹĒ
¢Ł»ģŗĻĪļ:ĀĮČČ¼Į”¢¼īŹÆ»Ņ”¢Ė®²£Į§”¢ĘÆ°×·Ū £» ¢Ś»ÆŗĻĪļ:ĀČ»ÆøĘ”¢ÉÕ¼ī”¢±łĖ®»ģŗĻĪļ”¢µØ·Æ””
¢ŪĖįŠŌŃõ»ÆĪļ£ŗMn2O7”¢N2O3”¢SiO2”¢NO2 ¢Ü¼īŠŌŃõ»ÆĪļ:Na2O2”¢CuO”¢Al2O3”¢MgO””
¢ŻĶ¬ĖŲŅģŠĪĢå:C60”¢C70”¢½šøÕŹÆ”¢ŹÆÄ« ¢ŽĒæµē½āÖŹ£ŗAlCl3 ”¢ BaSO4 ”¢MgO”¢ Ba(OH)2
A£®¢Ł¢Ś¢Ż¢Ž B£®¢Ś¢Ū¢Ü¢Ž C£®¢Ł¢Ś¢Ü¢Ż D£®¢Ł¢Ś¢Ü¢Ž
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģĢģ½ņŅ»ÖŠøßČż»Æѧ9ŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÓŠ¹ŲĻĀĮŠĶ¼Ź¾µÄŠšŹöÕżČ·µÄŹĒ£Ø£©
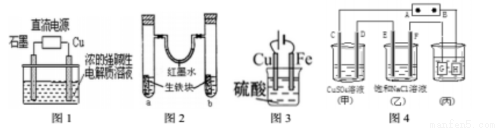
A£®Ķ¼1×Ü·“Ó¦ĪŖ£ŗ2Cu£«H2O Cu2O£«H2”üŌņĶµē¼«·¢Éś»¹Ō·“Ó¦£ŗ2Cu£«2OH££2e£=Cu2O£«H2O
Cu2O£«H2”üŌņĶµē¼«·¢Éś»¹Ō·“Ó¦£ŗ2Cu£«2OH££2e£=Cu2O£«H2O
B£®Ķ¼2ÖŠa”¢bŹŌ¹ÜÄŚ·Ö±šŹ¢ÓŠŹ³ŃĪĖ®ŗĶĀČ»Æļ§ČÜŅŗ£¬·ÅÖĆŅ»¶ĪŹ±¼äŗó£¬ŗģÄ«Ė®ÖłĮ½±ßµÄŅŗĆę±ä³É×óµĶÓŅøß
C£®Ķ¼3ÖŠĶµē¼«ÉĻ²»ÄܲśÉśĘųÅŻ
D£®Ķ¼4ÖŠC”¢D”¢E”¢F¶¼ŹĒ¶čŠŌµē¼«£¬ĻņŅŅÖŠµĪČė·ÓĢŖŹŌŅŗ£¬F¼«ø½½üĻŌŗģÉ«£¬ŌņÓūÓƱū×°ÖĆøųĶ¶ĘŅų£¬Ķ¼žÓ¦øĆĪŖG¼«
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģĖÄ“ØŹ”øßČżµŚČż“ĪĄķ×Ūæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠø÷·“Ó¦¶ŌÓ¦µÄĄė×Ó·½³ĢŹ½ÕżČ·µÄŹĒ£Ø £©
A£®“ĪĀČĖįÄĘČÜŅŗÖŠĶØČė¹żĮ涞Ńõ»ÆĮņClO£ + H2O + SO2 = HClO + HSO3£
B£®ĻņĢ¼ĖįĒāÄĘČÜŅŗÖŠ¼ÓČė¹żĮæĒāŃõ»ÆøĘČÜŅŗ2HCO3££« Ca2£«£«2OH£= CaCO3”ż£«2H2O£«CO32£
C£®ĒāŃõ»Æ±µČÜŅŗÓėĮņĖįČÜŅŗ·“Ó¦µĆµ½ÖŠŠŌČÜŅŗBa2£«£«OH££« H£«£«SO42”Ŗ = BaSO4”ż£«H2O
D£®50 mL 1mol/LµÄNaOHČÜŅŗÖŠĶØČė0.03 mol H2S 5OH£ + 3H2S = HS”Ŗ + 2S2£ + 5H2O
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com