
碱式硫酸铁[Fe(OH)SO4]是一种用于污水处理的新型高效絮凝剂,在医药上也可用于治疗消化性溃疡出血。工业上利用废铁屑(含少量氧化铝、氧化铁等)生产碱式硫酸铁的工艺流程如下。

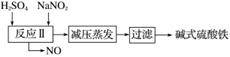
已知:部分阳离子以氢氧化物形式沉淀时溶液的pH如表所示。
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Al(OH)3 |
| 开始沉淀 | 2.3 | 7.5 | 3.4 |
| 完全沉淀 | 3.2 | 9.7 | 4.4 |
回答下列问题。
(1)加入少量NaHCO3的目的是调节pH,使溶液中的______沉淀,该工艺中“搅拌”的作用是__________。
(2)在实际生产中,反应Ⅱ中常同时通入O2以减少NaNO2的用量,O2与NaNO2在反应中均作________。若参与反应的O2有11.2 L(标准状况),则相当于节约NaNO2的物质的量为________。
(3)碱式硫酸铁溶于水后产生的Fe(OH)2+可部分水解生成聚合离子Fe2(OH)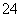 。该水解反应的离子方程式为__________________。
。该水解反应的离子方程式为__________________。
(4)在医药上常用硫酸亚铁与硫酸、硝酸的混合液反应制备碱式硫酸铁。根据我国质量标准,产品中不得含有Fe2+及NO 。为检验所得产品中是否含有Fe2+,应使用的试剂为________(填字母)。
。为检验所得产品中是否含有Fe2+,应使用的试剂为________(填字母)。
A.氯水 B.KSCN溶液
C.NaOH溶液 D.酸性KMnO4溶液
答案 (1)Al3+ 加快反应速率 (2)氧化剂 2 mol
(3)2Fe(OH)2++2H2O??Fe2(OH)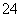 +2H+
+2H+
(4)D
解析 (1)废铁屑中含有氧化铝,反应Ⅰ中引入了杂质Al3+,加入NaHCO3调节pH至4.4可使Al3+完全沉淀。“搅拌”的目的是使反应物充分接触,从而加快化学反应速率。(2)硫酸亚铁溶液中加入NaNO2得到Fe(OH)SO4,铁的化合价升高而N的化合价降低,故NaNO2在反应中作氧化剂。1 mol O2可得到4 mol电子,1 mol NaNO2可得到1 mol电子,标况下11.2 L O2的得电子能力与2 mol NaNO2相当。(4)Fe2+能使酸性高锰酸钾溶液褪色,故可用酸性KMnO4溶液检验产品中是否含有Fe2+。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
下列各组物质不互为同分异构体的是( )
A.2,2二甲基丙醇和 2甲基丁醇
B.邻氯甲苯和对氯甲苯
C.2甲基丁烷和戊烷
D.甲基丙烯酸和甲酸丙酯
查看答案和解析>>
科目:高中化学 来源: 题型:
关于FeCl3进行的实验,下列预测正确的是( )
| 选项 | 实验 | 预测 |
| A | 蒸发FeCl3溶液 | 得到FeCl3固体 |
| B | 在FeCl3、CuCl2混合液中,加入少量Fe粉 | 一定有H2产生且有Cu析出 |
| C | 用FeCl3固体溶于水配制饱和溶液 | 会有Fe(OH)3沉淀产生 |
| D | 在FeCl3溶液中加入KHCO3溶液 | 有CO2产生,但无Fe(OH)3沉淀生成 |
查看答案和解析>>
科目:高中化学 来源: 题型:
FeCl3在现代工业生产中应用广泛。某化学研究性学习小组模拟工业流程制备无水FeCl3,再用副产品FeCl3溶液吸收有毒的H2S。
Ⅰ.经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华。他们设计了制备无水FeCl3的实验方案,装置示意图(加热及夹持装置略去)及操作步骤如下:
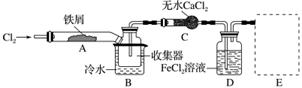
①检验装置的气密性;
②通入干燥的Cl2,赶尽装置中的空气;
③用酒精灯在铁屑下方加热至反应完成;
④……
⑤体系冷却后,停止通入Cl2,并用干燥的N2赶尽Cl2,将收集器密封。
请回答下列问题:
(1)装置A中反应的化学方程式为_________________________________________。
(2)第③步加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A右端。要使沉积的FeCl3进入收集器,第④步操作是_____________________________________。
(3)操作步骤中,为防止FeCl3潮解所采取的措施有(填步骤序号)____________。
(4)装置B中冷水浴的作用为__________________________________________________;
装置C的名称为________;装置D中FeCl2全部反应后,因失去吸收Cl2的作用而失效,写出检验FeCl2是否失效的试剂:_____________________________________________________。
Ⅱ.该组同学用装置D中的副产品FeCl3溶液吸收H2S,得到单质硫;过滤后,再以石墨为电极,在一定条件下电解滤液。
(6)FeCl3与H2S反应的离子方程式为________________________________________
________________________________________________________________________。
(7)电解池中H+在阴极放电产生H2,阳极的电极反应式为____________________________。
(8)综合分析实验 Ⅱ 的两个反应,可知该实验有两个显著优点:
①H2S的原子利用率为100%;
②________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将3.48 g四氧化三铁完全溶解在100 mL 1 mol·L-1的硫酸中,然后加入K2Cr2O7溶液25 mL,恰好使溶液中的Fe2+全部转化为Fe3+,Cr2O 全部转化为Cr3+,则K2Cr2O7溶液的物质的量浓度是( )
全部转化为Cr3+,则K2Cr2O7溶液的物质的量浓度是( )
A.0.05 mol·L-1 B.0.1 mol·L-1
C.0.2 mol·L-1 D.0.3 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
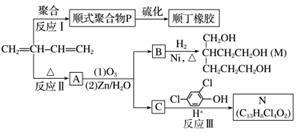
已知丙烷的分子结构可简写成键线式结构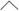 。有机物A的键线式结构为
。有机物A的键线式结构为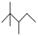 ,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是( )
,有机物B与等物质的量的H2发生加成反应可得到有机物A。下列有关说法错误的是( )
A.有机物A的一氯代物只有4种
B.用系统命名法命名有机物A,名称为2,2,3三甲基戊烷
C.有机物A的分子式为C8H18
D.B的结构可能有3种,其中一种名称为3,4,4三甲基?2?戊烯
查看答案和解析>>
科目:高中化学 来源: 题型:
顺丁橡胶、制备醇酸树脂的原料M以及杀菌剂N的合成路线如下:
已知:ⅰ.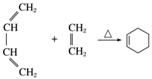
ⅱ.RCH===CHR′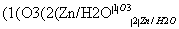 RCHO+R′CHO(R、R′代表烃基或氢)
RCHO+R′CHO(R、R′代表烃基或氢)
(1)CH2===CH—CH===CH2的名称是______________。
(2)反应Ⅰ的反应类型是(选填字母)________。
a.加聚反应 b.缩聚反应
(3)顺式聚合物P的结构式是(选填字母)________。

(4)A的相对分子质量为108。
①反应Ⅱ的化学方程式是__________________________________________________。
②1 mol B完全转化成M所消耗H2的质量是______g。
(5)反应Ⅲ的化学方程式是______________________________________________。
(6)A的某些同分异构体在相同的反应条件下也能生成B和C。写出其中一种同分异构体的结构简式________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化锌为白色粉末,可用于湿疹、癣等皮肤病的治疗。纯化工业级氧化锌[含有Fe(Ⅱ)、Mn(Ⅱ)、Ni(Ⅱ)等杂质]的流程如下:

滤液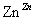
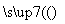 滤液
滤液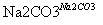
 滤饼
滤饼 ZnO
ZnO
提示:在本实验条件下,Ni(Ⅱ)不能被氧化;高锰酸钾的还原产物是MnO2。
回答下列问题:
(1)反应②中除掉的杂质离子是__________,发生反应的离子方程式为__________;在加高锰酸钾溶液前,若pH较低,对除杂的影响是________________。
(2)反应③的反应类型为____________,过滤得到的滤渣中,除了过量的锌外还有______________。
(3)反应④形成的沉淀要用水洗,检验沉淀是否洗涤干净的方法是________________。
(4)反应④中产物的成分可能是ZnCO3·xZn(OH)2,取干燥后的滤饼11.2 g,煅烧后可得到产品8.1 g,则x等于__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com