
【题目】美国科学家将两种元素铅和的原子核对撞,获得一种质子数为118,质量数为293的超重元素,该元素原子核内的中子数和核外电子数之差为
A.57B.118C.175D.293
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】铜器久置,表面会生成一层绿色固体,为了解铜在空气中的腐蚀情况,某化学兴趣小组收集家中铜器表面的绿色固体进行探究.查阅相关资料后,猜想该绿色物质可能是铜的碳酸盐. 该小组同学利用如图装置进行实验.
①对试管内的绿色固体进行加热,至完全分解,观察到A装置中绿色固体逐渐变成黑色,B装置中无水硫酸铜变成蓝色,C装置中澄清石灰水变浑浊.
②取少量加热后生成的黑色固体于试管中,加入稀硫酸.观察到黑色固体逐渐溶解,溶液变成蓝色.
③取少量上述蓝色溶液加入试管中,浸入一根洁净的铁丝.观察到铁丝表面有红色物质析出.
请回答下列问题:
(1)绿色固体中含有的元素是 .
(2)加热后试管中剩余的黑色物质是 .
(3)假设该绿色物质是一种纯净物,则其化学式可能是 , 加热分解的化学方程式为 .
(4)上述实验步骤③中的反应的离子方程式为 .
(5)实验装置最后的干燥管的作用是 .
(6)如果将B、C两装置对调,能否达到实验目的? , 为什么? .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中正确的是( )
A.NH3、CO,CO2都是极性分子
B.CH4、CCl4都是含有极性键的非极性分子
C.HF,HCl、HBr、HI的稳定性依次增强
D.CS2、H2O,C2H2都是直线形分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某Na2O2 固体中因吸收CO2 而含有少量Na2CO3,经实验测定样品中Na2O2的质量分数为88.0%。现称取该样品8.86g,加入水充分反应后放出气体,所得溶液体积为500mL。试计算:(要求:写出解题过程,计算结果保留两位小数)
(1)上述反应所得气体在标准状况下的体积;_________
(2)反应后溶液中Na+的物质的量浓度。_______________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由物质a为原料,制备物质d (金刚烷)的合成路线如下图所示: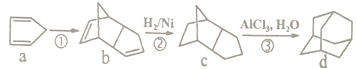
关于以上有机物说法中错误的是( )
A.物质a的分子式为C5H6
B.物质b使酸性高锰酸钾溶液和溴水褪色的原理相同
C.物质c与物质d互为同分异构体
D.物质d的一氯代物有2种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,三种碳酸盐MCO3(M:Mg2+、Ca2+、Mn2+)的沉淀溶解平衡曲线如图所示.已知:pM=﹣lgc(M),p(CO32﹣)=﹣lgc(CO32﹣).下列说法正确的是( ) 
A.MgCO3、CaCO3、MnCO3的Ksp依次增大
B.a点可表示MnCO3的饱和溶液,且c(Mn2+)>c(CO32﹣)
C.b点可表示CaCO3的饱和溶液,且c(Ca2+)<c(CO32﹣)
D.c点可表示MgCO3的不饱和溶液,且c(Mg2+)>c(CO32﹣)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是实验室制备氯气并进行一系列相关实验的装置(夹持设备已略)。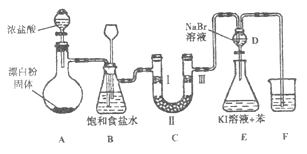
(1)装置A是氯气的发生装置,请写出该反应相应的化学方程式:。
(2)装置B中饱和食盐水的作用是;同时装置B也是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象:。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中I、Ⅱ、Ⅲ处依次放入物质的组合应是(填字母编号)。
编号 | I | Ⅱ | Ⅲ |
a | 干燥的有色布条 | 碱石灰 | 湿润的有色布条 |
b | 干燥的有色布条 | 无水硫酸铜 | 湿润的有色布条 |
c | 湿润的有色布条 | 浓硫酸 | 干燥的有色布条 |
d | 湿润的有色布条 | 无水氯化钙 | 干燥的有色布条 |
(4)设计装置D、E的目的是比较氯、溴、碘单质的氧化性。反应一段时间后,打开活塞,将装置D中少量溶液加入装置E中,振荡,观察到的现象是 , 该现象(填“能”或“不能”) 说明溴单质的氧化性强于碘,原因是。
(5)装置F的烧杯中的溶液不能选用下列中的(填字母编号)。a.饱和NaOH溶液 b.饱和Ca(OH)2溶液 c.饱和Na2CO3溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意解答
(1)某温度下,在Ca(OH)2(Ksp=5.5×10﹣6)、Mg(OH)2(Ksp=3.2×10﹣11)、AgCl(Ksp=1.8×10﹣10)三种物质中,溶解度最小的是
(2)在粗制CuSO45H2O晶体中常含有杂质Fe2+ . 在提纯时为了除去Fe2+ , 常加入氧化剂,使Fe2+氧化为Fe3+ , 下列物质最合适的是 A.KMnO4 B.H2O2 C.Cl2 水 D.HNO3
已知KMnO4氧化Fe2+时,生成Mn2+离子,试写出酸性KMnO4与Fe2+反应的离子反应方程式;然后再加入适当物质调整至溶液pH=4,使Fe3+转化为Fe(OH)3 , 可以达到除去Fe3+而不损失CuSO4的目的,调整溶液pH可选用下列中的
A.NaOH B. NH3H2O C.CuCO3 D.Cu(OH)2
(3)甲同学怀疑调整至溶液pH=4是否能达到除去Fe3+而不损失Cu2+的目的,乙同学认为可以通过计算确定,他查阅有关资料得到如下数据,常温下Fe(OH)3的溶度积Ksp=8.0×10﹣38 , Cu(OH)2的溶度积Ksp=3.0×10﹣18 , 通常认为残留在溶液中的离子浓度小于1×10﹣5 molL﹣1时就认为沉淀完全,设溶液中CuSO4的浓度为3.0molL﹣1 , 则Cu(OH)2开始沉淀时溶液的pH为 , Fe3+完全沉淀时溶液的pH为(已知lg2=0.3,lg5=0.7),通过计算确定上述方案(填“可行”或“不可行”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、D、E、W是中学常见的四种元素,原子序数依次增大。A的原子最外层电子数是次外层的2倍,D的氧化物属于两性氧化物,D、E位于同周期,A、D、E的原子最外层电子数之和为14,W是人体必需的微量元素,缺乏W会导致贫血症状。
(1)A在元素周期表中的位置是。
(2)下列事实能用元素周期律解释的是(填字母序号)。
a . D的最高价氧化物对应水化物的碱性弱于Mg(OH)2
b. E的气态氢化物的稳定性小于HF
c. WE3的溶液可用于刻蚀铜制的印刷电路板
(3)E的单质可以从NaBr溶液中置换出Br2单质,从原子结构的角度解释其原因是。
(4)①工业上用电解法制备D的单质,反应的化学方程式为。
②家用“管道通”的有效成分是烧碱和D的单质,使用时需加入一定量的水,此时发生反应的化学方程式为。
(5)W的单质可用于处理酸性废水中的NO3- , 使其转换为NH4+ , 同时生成有磁性的W的氧化物X,再进行后续处理。
① 上述反应的离子方程式为。
② D的单质与X在高温下反应的化学方程式为。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com