
【题目】为了测定铁铜合金的组成,将15.2 g铁铜合金加入200 mL某浓度的稀硝酸中,待合金完全溶解,共生成NO气体4.48 L(标准状况下),并测得溶液中H+的物质的量浓度为0.5 mol·L-1,若反应前后溶液的体积变化忽略不计
(1)n(Fe)=_________n(Cu)=_________
(2)硝酸的物质的量浓度为______________
【答案】n(Fe)=0.1 mol n(Cu)=0.15 mol c(HNO3)=4.5 mol/L
【解析】
通常列方程组解答混合物的计算问题,假设混合物中各组分的物质的量有利于找出等量关系。质量守恒、电荷守恒、氧化还原反应中得失电子守恒,都是列方程的重要依据。
(1)铁铜合金完全溶于稀硝酸后有H+剩余(即HNO3过量),则Fe、Cu分别被氧化为Fe3+、Cu2+。设合金中铁、铜的物质的量分别为x、y,则有①:56g/mol×x+64g/mol×y=15.2g。据得失电子守恒得②:3x+2y=![]() 。解①②得x=0.1 mol,y=0.15 mol。
。解①②得x=0.1 mol,y=0.15 mol。
(2)参加反应的HNO3中,作氧化剂(HNO3——NO)的为![]() =0.2mol,作酸(Fe——3HNO3,Cu——2HNO3)的为3x+2y=0.6mol。反应后剩余的HNO3为0.5mol/L×0.2L=0.1mol。原硝酸的物质的量浓度为(0.2mol+0.6mol+0.1mol)/0.2L=4.5 mol/L。
=0.2mol,作酸(Fe——3HNO3,Cu——2HNO3)的为3x+2y=0.6mol。反应后剩余的HNO3为0.5mol/L×0.2L=0.1mol。原硝酸的物质的量浓度为(0.2mol+0.6mol+0.1mol)/0.2L=4.5 mol/L。


科目:高中化学 来源: 题型:
【题目】一定条件下,下列反应中水蒸气含量随反应时间的变化趋势符合题图10 的是
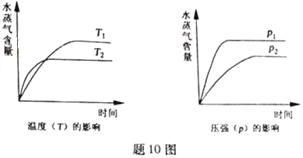
A. CO2(g)+2NH3(g)![]() CO(NH2)2(s)+H2O(g);△H<0
CO(NH2)2(s)+H2O(g);△H<0
B. CO2(g)+H2(g)![]() CO(g)+H2O(g);△H>0
CO(g)+H2O(g);△H>0
C. CH3CH2OH (g)![]() CH2=CH2(g)+H2O(g);△H>0
CH2=CH2(g)+H2O(g);△H>0
D. 2C6H5CH2CH3(g)+O2(g)![]() 2 C6H5CH=CH2(g)+2H2O(g);△H<0
2 C6H5CH=CH2(g)+2H2O(g);△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列与有机物的结构、性质有关的叙述不正确的是
A. 乙醇、乙烯均能使酸性KMnO4溶液褪色
B. 光照下甲烷和Cl2的反应、在FeBr3催化下苯和Br2的反应属于同一类型的反应
C. 甲醇、醋酸均能与Na反应放出H2,但二者所含官能团不相同
D. 甲苯的一氯代物的同分异构体有三种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】[化学-—选修3:物质结构与性质]东晋《华阳国志南中志》卷四中已有关于白铜的记载,云南镍白铜(铜镍合金)闻名中外,曾主要用于造币,亦可用于制作仿银饰品。回答下列问题:
(1)镍元素基态原子的电子排布式为_________,3d能级上的未成对的电子数为______。
(2)硫酸镍溶于氨水形成[Ni(NH3)6]SO4蓝色溶液。
①[Ni(NH3)6]SO4中阴离子的立体构型是_____。
②在[Ni(NH3)6]2+中Ni2+与NH3之间形成的化学键称为______,提供孤电子对的成键原子是_____。
③氨的沸点(填“高于”或“低于”)膦(PH3),原因是______;氨是_____分子(填“极性”或“非极性”),中心原子的轨道杂化类型为_______。
(3)单质铜及镍都是由______键形成的晶体:元素铜与镍的第二电离能分别为:ICu=1959kJ/mol,INi=1753kJ/mol,ICu>INi的原因是______。
(4)某镍白铜合金的立方晶胞结构如图所示。

①晶胞中铜原子与镍原子的数量比为_____。
②若合金的密度为dg/cm3,晶胞参数a=________nm。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1.28g铜投入一定量的浓硝酸中,铜完全溶解,生成气体颜色越来越浅,共收集到VmL气体(标准状况),将盛有此气体的容器倒扣在水中,通入氧气恰好使气体完全溶解在水中,则需要标准状况下的氧气体积为( )
A. 504mLB. 336mLC. 224mLD. 168mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于价层电子对互斥模型(VSEPR模型)和杂化轨道理论的叙述中正确的是
A. 凡是中心原子采取sp2杂化的分子,其分子构型都是平面三角形
B. 对于主族元素,中心原子的杂化轨道数等于价层电子对数
C. 杂化轨道可用于形成![]() 键、π键或用于容纳未参与成键的弧电子对
键、π键或用于容纳未参与成键的弧电子对
D. Sp3杂化轨道是由任意的1个s轨道和3个p轨道杂化形成的四个sp3杂化轨道
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种降血脂药物吉非罗齐(W)的结构简式为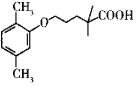 ,一种合成W的路线如下:
,一种合成W的路线如下:
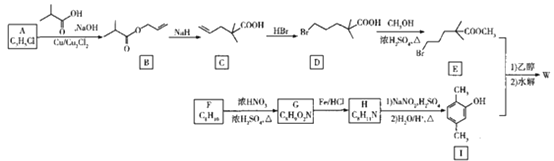
已知:
![]()
回答下列问题:
(1)A的化学名称是______。
(2)C生成D、D生成E的反应类型依次是______、______。
(3)F生成G的化学方程式为______。
(4)H的结构简式为______,W的分子式为______。
(5)X是B的一种同分异构体且所含的官能团完全相同,其核磁共振氢谱有3组峰,面积比为9:2:1,写出一种符合要求的X的结构简式:______。
(6)间苯三酚羧酸( )是一种医药中间体,参照上述合成路线设计以甲苯为起始原料制备间苯三酚羧酸的合成路线:______(无机试剂任用)。
)是一种医药中间体,参照上述合成路线设计以甲苯为起始原料制备间苯三酚羧酸的合成路线:______(无机试剂任用)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个不传热的固定容积的密闭容器中,可逆反应mA(g)+nB(s)![]() pC(g)+qD(g),当m、n、p、q为任意整数时,一定说明达到平衡的是( )
pC(g)+qD(g),当m、n、p、q为任意整数时,一定说明达到平衡的是( )
①体系的压强不再改变 ②体系的温度不再改变 ③B的浓度不再改变 ④各组分的质量分数不再改变 ⑤反应速率v(A):v(C):v(D)=m:p:q ⑥单位时间内m mol A发生断键反应,同时p mol C也发生断键反应
A.④⑤⑥B.②④⑥C.①④⑤D.①③⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某有机物的结构如图所示,下列说法正确的是
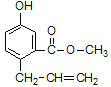
A. 该有机物的分子式为C11H11O3
B. 1 mol该有机物最多能和5 mol H2发生加成反应
C. 该有机物能与碳酸氢钠溶液反应
D. 一定条件下和浓溴水反应时,1 mol 该有机物能消耗3 mol Br2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com