
| A. | ${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、H+和H2是氢元素的四种不同粒子 | |
| B. | ${\;}_{20}^{40}$Ca和 ${\;}_{20}^{42}$Ca、石墨和金刚石均为同位素 | |
| C. | ${\;}_{1}^{1}$H和 ${\;}_{1}^{2}$H是不同的核素 | |
| D. | 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同 |
分析 A.根据四种微粒符号表示的意义进行解答;
B.质子数相同中子数不同的同一元素的不同原子互称同位素;
C.核素是具有一定质子数和一定中子数的原子;
D.元素的原子的最外层电子数决定了元素性质,有相同质子数,不同中子数的原子互为同位素,互为同位素,物理性质不同,但化学性质几乎完全相同.
解答 解:A.${\;}_{1}^{1}$H、${\;}_{1}^{2}$H、H+和H2是分别表示:质子数为1中子数为0的氢原子、质子数为1,中子数为1的氢原子、带一个单位正电荷的氢离子、氢气单质,同属于氢元素的四种不同粒子,故A正确;
B.同一元素的不同原子互称同位素,${\;}_{20}^{40}$Ca和 ${\;}_{20}^{42}$Ca都是Ca元素的不同原子,所以互称同位素,金刚石、石墨都是由碳元素组成的不同单质,不属于同位素,故B错误;
C.${\;}_{1}^{1}$H和 ${\;}_{1}^{2}$H的质子数均为1,中子数不同,是不同的核素,故C正确;
D.有相同质子数,不同中子数的原子互为同位素,元素的原子的最外层电子数决定了元素性质,而同位素的外层电子数相等,所以它们的化学性质几乎完全相同,而原子不同,则物理性质不同,12C和14C质子数都为6,互为同位素,物理性质不同,但化学性质几乎完全相同,故D正确;
故选B.
点评 本题考查了微粒符号表示的意义,题目难度不大,明确质子数、中子数、质量数、核外电子数之间的关系以及元素符号的左下角表示质子数,左上角表示质量数是解答本类题型的关键,注意互为同位素,物理性质不同,但化学性质几乎完全相同是高频考点.


 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:解答题
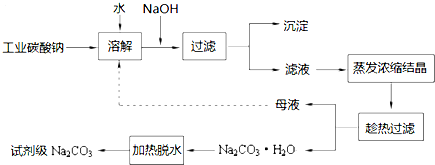
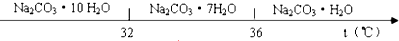
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 医用酒精消毒的原理是将病毒氧化达到消毒目的 | |
| B. | 加热消毒是因为高温下蛋白质发生了变性 | |
| C. | 自来水净化过程中加入明矾的作用是消毒杀菌 | |
| D. | 使用84消毒液(有效成分次氯酸钠)时通入CO2或SO2均可增强消毒效果 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
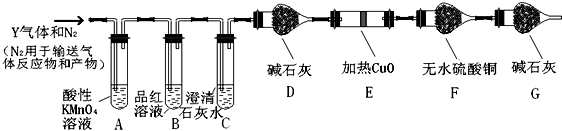 (2)写出产生CO2的化学方程式C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O.
(2)写出产生CO2的化学方程式C+2H2SO4(浓) $\frac{\underline{\;\;△\;\;}}{\;}$ CO2↑+2SO2↑+2H2O.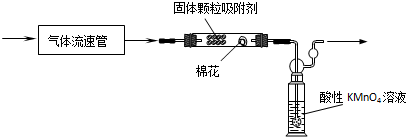
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. 查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 测定新制氯水pH,用玻璃棒蘸取液体滴在pH试纸上,与标准比色卡对照即可 | |
| B. | 做蒸馏实验时,在蒸馏烧瓶中应加入沸石,以防暴沸.如果在沸腾前发现忘记加沸石,应立即停止加热,冷却后补加 | |
| C. | 稀盐酸可除去烧瓶内残留的MnO2 | |
| D. | 根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
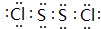 ;该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液.试写出该过程的化学方程式:2S2Cl2+2H2O=3S+SO2↑+4HCl;
;该物质遇水不稳定,生成一种黄色沉淀和无色气体,还得到一种酸性溶液.试写出该过程的化学方程式:2S2Cl2+2H2O=3S+SO2↑+4HCl;查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com