
| A. | 氧气和臭氧互为同素异形体 | |
| B. | CH3-CH2OH和 CH3-O-CH3互为同分异构体 | |
| C. | ${\;}_{2}^{3}$ He和${\;}_{2}^{4}$He互为同位素 | |
| D. | ${\;}_{2}^{4}$ He的最外层电子数为2,所以${\;}_{2}^{3}$He具有较强的金属性 |
分析 A.同种元素形成的不同单质互为同素异形体;
B.分子式相同,结构不同的化合物互称为同分异构体;
C.质子数相同中子数不同的原子互称同位素;
D.${\;}_{2}^{4}$ He的最外层电子数为2,为稳定结构.
解答 解:A.O2和O3是氧元素组成的结构不同的单质,互为同素异形体,故A正确;
B.CH3-CH2OH和 CH3-O-CH3分子式相同,结构不同,互为同分异构体,故B正确;
C.${\;}_{2}^{3}$ He和${\;}_{2}^{4}$HeHe中子数不同,是氢元素的不同原子,互为同位素,故C正确;
D.${\;}_{2}^{4}$ He的最外层电子数为2,难以失去电子,金属性较弱,故D错误;
故选D.
点评 本题主要考查了同系物、同分异构体、同位素、同素异形体的区别,难度不大,注意把握概念的内涵与外延.


科目:高中化学 来源: 题型:选择题
 自然界中金属硫化物之间存在原电池反应,下图所示装置中电极I为方铅矿(PbS),电极Ⅱ为含有方铅矿的硫铁矿,当有电解质溶液按如图所示方向流经该装置时,电流表指针偏转.若电极Ⅱ质量不断减少,a处溶液中加入KSCN溶液未出现红色,加入CuSO4溶液未出现黑色沉淀.下列有关说法中正确的是( )
自然界中金属硫化物之间存在原电池反应,下图所示装置中电极I为方铅矿(PbS),电极Ⅱ为含有方铅矿的硫铁矿,当有电解质溶液按如图所示方向流经该装置时,电流表指针偏转.若电极Ⅱ质量不断减少,a处溶液中加入KSCN溶液未出现红色,加入CuSO4溶液未出现黑色沉淀.下列有关说法中正确的是( )| A. | 工业上利用该原理富集铁 | |
| B. | 电极Ⅱ作正极 | |
| C. | 溶液流经该装置后pH增大 | |
| D. | 该装置负极的电极反应为FeS2-15e-+8H2O=Fe3++2SO42-+16H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
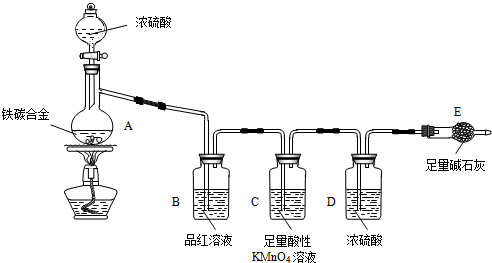
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
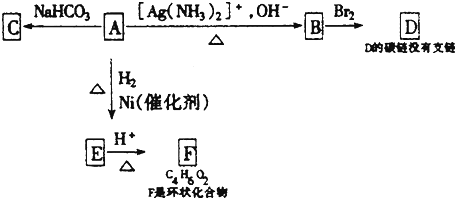
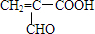 .
.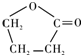 .由E生成F的反应类型是酯化反应.
.由E生成F的反应类型是酯化反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧气是氧化产物 | |
| B. | O2F2既是氧化剂又是还原剂 | |
| C. | 若生成4.48LHF,则转移0.8mol电子 | |
| D. | 还原剂与氧化剂的物质的量之比为1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 二氧化碳的结构式:O-C-O | B. | 过氧化钠的电子式: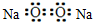 | ||
| C. | 丙烷分子的球棍模型: | D. | Cl-的结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
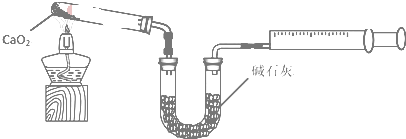
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子半径:Y>Z>W | |
| B. | Z的最高价氧化物的水化物为强酸 | |
| C. | 非金属性最强的元素为W | |
| D. | XW2分子中各原子最外层电子均达到8电子结构 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com