
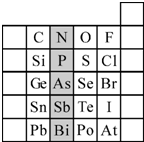


分析 (1)阴影部分元素处于ⅤA族,最外层还有5个电子,据此写出其外围电子排布的通式;根据P所在周期表中位置判断其结构及电子占据的最高层符号;M层还有s、p、d轨道,据此计算还有轨道数;Se的元素名称为硒;
(2)a.非金属性越强,氢化物的稳定性越强;
b.由于氨气分子间存在氢键,因此氨气的沸点最高,AsH3的相对分子质量大于PH3,AsH3沸点较高;
c.非金属性越强与氢元素形成的共价键越强,键能越大;
d.三种氢化物生成的晶体均是分子晶体,分子间作用力随相对分子质量的增加而增大;
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是亚硝酸;酸根呈三角锥结构,说明该酸根离子价层电子对个数是4且含有一个孤电子对;
(4)氢、氮、氧、硫、铜这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,说明该阴离子价层电子对个数是4且不含孤电子对;
阳离子中存在共价键和配位键;H2O和Cu2+的配位键比NH3与Cu2+的弱,所以该化合物加热时首先失去的组分是H2O
(5)SiO44-中价层电子对个数是4且不含孤电子对,利用均摊法计算其原子个数比,从而确定其化学式.
解答 解:(1)阴影部分元素处于ⅤA族,最外层还有5个电子,其外围电子排布的通式为:ns2np3;P核外还有3个电子层,则电子占据的最高层符号为M,M层还有1个s轨道、3个p轨道和5个d轨道,总共还有9个轨道;Se元素为硒,
故答案为:ns2np3;M;9;硒;
(2)a.N、P、As位于周期表同一主族,从上到下排列,根据元素周期律可知,非金属性越强,氢化物的稳定性越强,因此三种氢化物的稳定性逐渐降低,a正确;
b.由于氨气分子间存在氢键,因此氨气的沸点最高,AsH3的相对分子质量大于PH3,AsH3沸点较高,故b错误;
c.非金属性越强与氢元素形成的共价键越强,键能越大,因此R-H键能随原子序数的增大而减小,故c正确;
d.三种氢化物生成的晶体均是分子晶体,分子间作用力随相对分子质量的增加而增大,故d错误;
故答案为:ac;
(3)这些元素形成的含氧酸中,分子的中心原子的价层电子对数为3的酸是HNO2、HNO3;酸根呈三角锥结构的酸是H2SO3,
故答案为:HNO2、HNO3;H2SO3;
(4)氢、氮、氧、硫、铜这5种元素形成的一种1:1型离子化合物中,阴离子呈四面体结构,说明该阴离子价层电子对个数是4且不含孤电子对,为SO42-;
H2O和Cu2+的配位键比NH3与Cu2+的弱,所以该化合物加热时首先失去的组分是H2O,
故答案为:SO42-;H2O;H2O和Cu2+的配位键比NH3与Cu2+的弱;
(5)根据图片知,每个三角锥结构中P原子是1个,O原子个数=2+2×$\frac{1}{2}$=3,所以P原子和氧原子个数之比=1:3,3个O原子带6个单位负电荷,每个P原子带4个单位正电荷,所以形成离子为[PO3]n2n- (或PO32-),
故答案为:PO32-(或(PO3)n2n-).
点评 本题考查了位置、结构与性质关系的综合应用,题目难度中等,明确原子结构与元素周期表、元素周期律的关系为解答关键,试题知识点较多、综合性较强,充分培养了学生的分析能力及灵活运用能力.


 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案科目:高中化学 来源: 题型:选择题
| A. | CH2=CH2 | B. | CH3CH=CH2 | C. | CH3C≡CH | D. | CH3CH=CHCH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | $\frac{({C}_{1}+{C}_{2}){ρ}_{3}}{{ρ}_{1}+{ρ}_{2}}$ | B. | $\frac{{C}_{1}+{C}_{2}}{{ρ}_{1}+{ρ}_{2}}$ | ||
| C. | $\frac{({C}_{1}+{C}_{2}){ρ}_{3}}{1000({ρ}_{1}+{ρ}_{2})}$ | D. | $\frac{1000({C}_{1}+{C}_{2}){ρ}_{3}}{{ρ}_{1}+{ρ}_{2}}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 3 mL | B. | 2.5 mL | C. | 12.5 mL | D. | 17.5 mL |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 可用25mL碱式滴定管量取20.00mLKMnO4溶液 | |
| B. | 读取滴定管内液体的体积抑视会导致读数偏大 | |
| C. | 做中和滴定实验时,用待测液润洗锥形瓶 | |
| D. | 用盐酸标准溶液滴定待测的氢氧化钠溶液时,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 化学式 | 电离常数 |
| HF | K=3.5×10-4 |
| H2CO3 | K1=4.3×10-7 |
| K2=5.6×10-11 | |
| HClO | K=3.2×10-8 |
| A. | 酸性强弱:KClO>H2CO3>HF | |
| B. | 同温同浓度下,溶液的pH值:NaF>NaClO>Na2CO3 | |
| C. | 次氯酸钠溶液中通少量二氧化碳的离子方程式:ClO-+CO2+H2O═HCO3-+HClO | |
| D. | 碳酸钠溶液中加入少量氢氟酸的离子方程式:CO${{\;}_{3}}^{2-}$+2HF═2F-+H2O+CO2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| T/K | T1 | 573 | T2 |
| K | 1.00×107 | 2.45×105 | 1.88×103 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com