
 在2L的密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:
在2L的密闭容器内,800℃时反应2NO(g)+O2(g)?2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)(mol) | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
| △c |
| △t |
| 0.020mol-0.007mol |
| 2L |
| ||
| △t |
| ||
| 2s |
| 1 |
| 2 |
| 1 |
| 2 |


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
| A、FeCl3 溶液与铁反应:Fe+Fe3+═2Fe2+ |
| B、向Ca(HCO3)2溶液中加入足量NaOH溶液:Ca2++HCO3-+OH-=CaCO3↓+H2O |
| C、铝粉溶于NaOH溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑ |
| D、金属钠跟水反应Na+2H2O═Na++OH-+H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A | ||||||
| D | E | F | H | |||
| C | B | G |
查看答案和解析>>
科目:高中化学 来源: 题型:
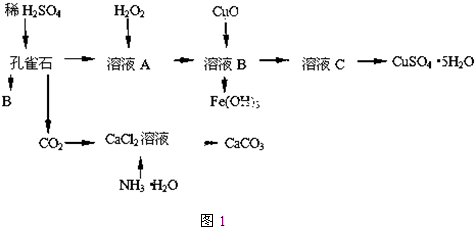
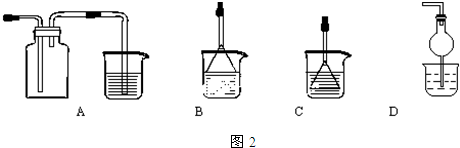
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba2+ |
| B、NH4+ |
| C、K+ |
| D、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH计能用于酸碱中和滴定终点的判断 | ||||
| B、NH4Cl水解反应:NH4++2H2O?NH3?H2O+H3O+ | ||||
| C、①pH=2的CH3COOH ②pH=2的盐酸 ③pH=12的氨水 ④pH=12的NaOH四种溶液,在相同温度下,水电离的出来的c(H+):①=②=③=④ | ||||
D、用铜做电极电解AgNO3溶液的离子方程:4Ag++2H2O
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com