
 +______MnO
+______MnO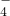 +______H+═______CO2↑+______Mn2++______H2O
+______H+═______CO2↑+______Mn2++______H2O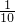 ,所以①、②中计算的数据均为配置溶液中溶质的
,所以①、②中计算的数据均为配置溶液中溶质的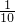 ,由①得:2n(H2C2O4?2H2O)+n(KHC2O4)=0.05mol,由②得:n(H2C2O4?2H2O)+n(KHC2O4)=0.04mol,
,由①得:2n(H2C2O4?2H2O)+n(KHC2O4)=0.05mol,由②得:n(H2C2O4?2H2O)+n(KHC2O4)=0.04mol,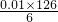 ×100%=21%;
×100%=21%;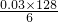 ×100%=64%;
×100%=64%;

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:山东省潍坊市第一中学2011届高三教学质量检测化学试题 题型:022
氧化还原反应中实际上包含氧化和还原两个过程,下面是一个还原过程的反应式:NO3-+4H++3e-→NO↑+2H2O.
KMnO4、Na2CO3、Cu2O、Fe2(SO4)3四种物质中的一种物质(甲)能使上述还原过程发生.请回答:
(1)写出该氧化还原反应的化学方程式(不必配平):________.
(2)反应中硝酸表现出________、________的性质.
(3)反应中若产生4.48 L(标准状况)气体,则转移电子的物质的量是________mol.
(4)硝酸浓度不同,与甲反应的产物不同.若1 mol甲与某浓度硝酸反应时,被还原硝酸的物质的量增加,原因是:________.
查看答案和解析>>
科目:高中化学 来源:2011-2012学年上海市高三上学期期中考试化学试卷 题型:填空题
H2O2是一种重要的氧化剂,亦具有还原性。下列① ~ ④个涉及H2O2的反应(未配平、条件略)。①Na2O2+ HCl→NaCl + H2O2 ②H2O2 →H2O + O2③Ag2O + H2O2 →Ag + O2 + H2O ④H2O2 + Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O。
据此,填写下列空白:(1)配平上述反应④,并标出电子转移方向与数目。
[ ]H2O2 +[ ]Cr2(SO4)3+[ ]KOH→[ ]K2CrO4+[ ]K2SO4+[ ]H2O
当0.1mol氧化剂参加反应时,转移电子个。
(2)H2O2仅体现还原性的反应是(填代号),此反应中的氧化产物为。
(3)H2O2体现弱酸性的反应是(填代号),其理由为。
查看答案和解析>>
科目:高中化学 来源: 题型:
H2O2是一种重要的氧化剂,亦具有还原性。下列① ~ ④个涉及H2O2的反应(未配平、条件略)。①Na2O2+ HCl→NaCl + H2O2 ②H2O2→H2O+ O2③Ag2O+ H2O2 →Ag + O2 + H2O ④H2O2 + Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O。
据此,填写下列空白:(1)配平上述反应④,并标出电子转移方向与数目。
[ ]H2O2 +[ ]Cr2(SO4)3+[ ]KOH→[ ]K2CrO4+[ ]K2SO4+[ ]H2O
当0.1mol氧化剂参加反应时,转移电子个。
(2)H2O2仅体现还原性的反应是(填代号),此反应中的氧化产物为。
(3)H2O2体现弱酸性的反应是(填代号),其理由为。
查看答案和解析>>
科目:高中化学 来源:2012届上海市南汇中学高三上学期期中考试化学试卷 题型:填空题
H2O2是一种重要的氧化剂,亦具有还原性。下列① ~ ④个涉及H2O2的反应(未配平、条件略)。①Na2O2+ HCl→NaCl + H2O2 ②H2O2 →H2O + O2③Ag2O + H2O2 →Ag + O2 + H2O ④H2O2 + Cr2(SO4)3+KOH→K2CrO4+K2SO4+H2O。
据此,填写下列空白:( 1)配平上述反应④,并标出电子转移方向与数目。
1)配平上述反应④,并标出电子转移方向与数目。
[ ]H2O2 +[ ]Cr2(SO4)3+[ ]KOH→[ ]K2CrO4+[ ]K2SO4+[ ]H2O
当0.1mol氧化剂参加反应时,转移电子个。
(2)H2O2仅体现还原性的反应是(填代号),此反应中的氧化产物为。
(3)H2O2体现弱酸性的反应是(填代号),其理由为。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com