
下列事实不能用化学平衡移动原理解释的是( )
A.光照新制的氯水时,溶液的pH逐渐减小
B.加催化剂,使N2和H2在一定条件下转化为NH3
C.可用浓氨水和氢氧化钠固体快速制取氨气
D.增大压强,有利于SO2与O2反应生成SO3
科目:高中化学 来源: 题型:
某硫酸厂以含有SO2的尾气、氨水等为原料,合成有重要应用价值的硫化钙、硫酸钾、亚硫酸铵等物质。合成路线如下:
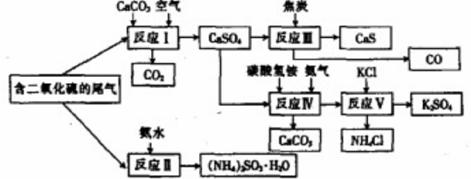
(1)写出反应Ⅲ的化学方程式:
(2)下列有关说法正确的是 (填字母)。
A反应Ⅰ中需鼓入足量空气,以保证二氧化硫充分氧化生成硫酸钙
B.反应Ⅱ和反应Ⅲ的基本反应类型相同
C.反应Ⅳ需控制在60-70℃,目的之一是减少碳酸氢铵的分解
D.反应Ⅴ中的副产物氯化铵可用作氮肥
(3) (NH4 )2SO3可用于电厂等烟道气中脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统。写出二氧化氮与亚硫酸铵反应的化学方程式: .
(4)很多硫酸厂为回收利用SO2,直接用氨水吸收法处理尾气.
①用15. 0mL 2.0mol·L-1氨水吸收标准状况下448 mL SO2,吸收液中的溶质为
②某同学用酸性KMnO4溶液滴定上述吸收液,当达到滴定终点时,消耗KMnO4溶液25. 00 mL,则酸性KMnO4溶液中,c(KMnO4)=
(5)氨气用途广泛,可以直接用于燃料电池,右图是用氨水作燃料的燃料电池的工作原理。

氨气燃料电池的电解质溶液最好选择 (填“酸性”“碱性”或“中性”)溶液,氮气燃料电池的反应是氨气与氧气生成一种常见的无毒气体和水,该电池总反应的化学方程式
是_______________________________,负极的电极反应式是_______________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
某中学化学兴趣小组为了调查当地某一湖泊的水质污染情况,在注入湖泊的3 个主要水源的入口处采集水样,并进行了分析,给出了如下实验信息:其中一处水源含有A、B两种物质,一处含有C、D两种物质,一处含有E物质,A、B、C、D、E为五种常见化合物,均由下表中的离子形成:
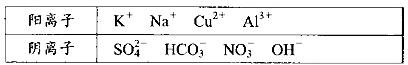
为了鉴别上述化台物。分别完成以下实验,其结果是:
①将它们溶于水后,D为蓝色溶液,其他均为无色溶液;
②将E溶液滴入到C溶液中出现白色沉淀,继续滴加,沉淀溶解;
③进行焰色反应,只有B、c为紫色(透过蓝色钻玻璃);
④在各溶液中加入硝酸锁溶液,再加过量稀硝酸,A中放出无色气体,C、D中都能产
生白色沉淀:
⑤将B、D两溶液混合,未见沉淀或气体生成。
根据上述实验填空:
(1)写出B、D的化学式:B________,D________。
(2)将含I mol A的溶液与含l molE的溶液反应后蒸于,仅得到一种化台物,该化合物的化学式为_____________.
(3)在A溶液中加入少量澄清石灰水,其离子方程式为________________。
(4)C常用作净水剂,用离子方程式和适当文字说明其净水原理_____________。
(5)若向含溶质lmol的C溶液中逐滴加入Ba(OH)2溶液,生成沉淀质量最大为______________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
2014 年 3 月 21 日是第二十二届“世界水日”,保护水资源,从我做起!
(1)ClO2和Cl2(还原产物都为Cl-)是生活中常用的消毒剂。当消耗等物质的量的两种物质时,ClO2的消毒效率是Cl2的____________倍。
2)某无色废水中可能含有 Fe3+、Al3+、Mg2+、Na+、NO-、CO32-、SO42-离子中的几种,为分析其成分,分别取废水样品 100 mL,进行了三组实验,其操作和有关现象如下图所示:
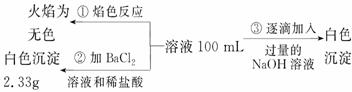
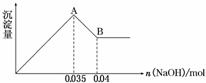
请根据上图回答下列问题:
①实验中需配制 1.0 mol/L的NaOH溶液100 mL,所需仪器除了玻璃棒、托盘天平、量筒、药匙、烧杯、胶头滴管, 还缺少的仪器为_________。
②实验③中沉淀量由 A→B过程中所发生反应的离子方程式为__________。
③试确定NO3-是否存在?_______(填“存在”、“不存在”或“不确定”),若存在,试计算 c(NO3-)=____________(若不存在,此问不必作答)。
查看答案和解析>>
科目:高中化学 来源: 题型:
在下列反应中:A2(g)+B2(g)2AB(g) ΔH<0当其达到平衡时,在下图所示的曲线中,符合勒夏特列原理的是( )
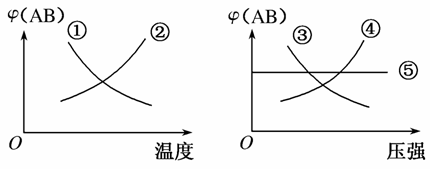
A.①② B.③④
C.① D.①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条下,在体积为2 L的密闭容器中,3mol X和3mol Y发生反应:
3X(g)+Y(g)2Z(g),经60 s达到平衡,生成0.4mol Z。下列说法正确的是( )
A.60 s内反应速率为v(X)=0.05mol/(L·s),X的转化率为80%
B.其他条件不变,将容器体积变为4 L,Z的平衡浓度变为原来的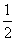
C.其他条件不变,若升高温度,X的体积分数增大,则该反应的ΔH>0
D.其他条件不变,若初始投入2mol X和2mol Y则物质Y的转化率减小
查看答案和解析>>
科目:高中化学 来源: 题型:
汽车尾气中的有毒气体NO和CO,在一定条件下可发生反应生成N2和CO2.下列关于此反应的说法中,正确的是()
A. 减小压强能增大反应速率
B. 增大压强能减小反应速率
C. 使用适当的催化剂能增大反应速率
D. 升高温度对反应速率无影响
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com