
| A. | C2H5OH(l)+3O2(g)=2CO2(g)+3H2O(g)△H=-1367.0kJ/mol (△H代表乙醇的燃烧热) | |
| B. | HCl (aq)+NaOH(aq)=NaCl(aq)+H2O(1)△H=-57.3kJ/mol (△H代表中和热) | |
| C. | 2H2O(g)=2H2(g)+O2(g)△H=+483.6 kJ/mol (反应热) | |
| D. | C(s)+O2(g)═CO2(g)△H=+393.5 kJ/mol (反应热) |
分析 A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量;
B、中和热是强酸强碱稀溶液中和反应生成1mol水时放出的热量;
C、热化学方程式中标注物质聚集状态,标明反应放出或是吸收的热量;
D、固体碳燃烧时放出热量,焓变是负值.
解答 解:A、燃烧热是1mol可燃物完全燃烧生成稳定氧化物放出的热量,反应中生成的水为气体不是稳定氧化物,故A错误;
B、中和热是强酸强碱稀溶液中和反应生成1mol水时放出的热量,该热化学方程式符合题意,故B正确;
C、2H2O(g)=2H2(g)+O2(g)△H=+483.6 kJ/mol (反应热)表明了水的分解过程以及所吸收的热量两个方面,故C正确;
D、固体碳燃烧时放出热量,焓变是负值,不是吸热的反应,故D错误.
故选BC.
点评 本题考查了热化学方程式书写方法,主要是燃烧热、中和热的概念理解和判断,注意热化学方程式书写方法和原则,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 保存硫酸亚铁溶液时,向其中加入铁钉和少量硫酸 | |
| B. | 少量金属钠保存在煤油中 | |
| C. | 少量液溴可用水封存,防止溴挥发 | |
| D. | 浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原混合物中铜和铁各0.15 mol | |
| B. | 稀硝酸的物质的量浓度为1 mol•L-1 | |
| C. | 第一次剩余9.6 g金属为铜和铁 | |
| D. | 再加入上述200 mL稀硝酸,还会得到标准状况下2.24 L NO |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
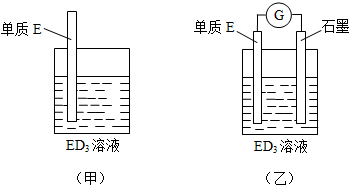
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
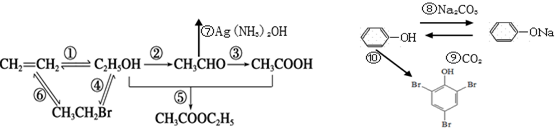
 ,取代反应.
,取代反应.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2分子的结构式:O=C=O | B. | 氮气的电子式: | ||
| C. | 钙离子的电子式:Ca2+ | D. | Na的原子结构示意图: |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 实验 编号 | T/℃ | 大理石 规格 | HNO3浓度 (mol?L-1) | 实验目的 |
| ① | 25 | 粗颗粒 | 2.00 | (Ⅰ)实验①和②探究HNO3浓度对该反应速率的影响; (Ⅱ)实验①和③探究温度对该反应速率的影响; (Ⅲ)实验①和④探究大理石规格(粗、细)对该反应速率的影响; |
| ② | ||||
| ③ | 粗颗粒 | 2.00 | ||
| ④ | 25 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 凡是分子组成相差一个或几个CH2原子团的物质,彼此一定是同系物 | |
| B. | 两种化合物组成元素相同,各元素质量分数也相同,则两者一定是同分异构体 | |
| C. | 相对分子质量相同的几种化合物,互称为同分异构体 | |
| D. | 组成元素的质量分数相同,且相对分子质量也相同的不同化合物,一定互为同分异构体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com