
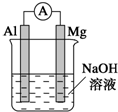
 将镁条、铝条平行插入一定浓度的NaOH溶液中,用导线和电流表连接成原电池.装置如图所示,此电池工作时,下列叙述中正确的是( )
将镁条、铝条平行插入一定浓度的NaOH溶液中,用导线和电流表连接成原电池.装置如图所示,此电池工作时,下列叙述中正确的是( )| A. | Mg比Al活泼,Mg失去电子被氧化成Mg2+ | |
| B. | 铝条表面虽有氧化膜,但可不必处理 | |
| C. | 正极反应式为2H++2e-═H2↑ | |
| D. | Al是电池负极,开始工作时溶液中会立即有白色沉淀析出 |
分析 A、金属镁和氢氧化钠溶液不能发生氧化还原反应;
B、铝片表面的氧化膜也能与NaOH溶液反应;
C、正极上水中的H元素得电子生成氢气;
D、铝离子在过量的碱性溶液中不会产生氢氧化铝沉淀.
解答 解:A、在NaOH溶液中,铝能与NaOH溶液发生氧化还原反应,在该反应中,铝失电子作原电池的负极,而属镁和氢氧化钠溶液不能发生氧化还原反应,故A错误;
B、由于铝片表面的氧化膜也能与NaOH溶液反应,故其不必处理,故B正确;
C、正极上水得电子发生还原反应,电极反应式为2H2O+2e-=H2↑+2OH-,故C错误;
D、在NaOH溶液中,铝能与NaOH溶液发生氧化还原反应,在该反应中,铝失电子作原电池的负极,由于电池开始工作时,生成的铝离子的量较少,NaOH过量,此时不会有Al(OH)3白色沉淀生成,故D错误.
故选B.
点评 本题考查了原电池原理,正确判断原电池正负极是解本题关键,根据各个电极上发生的反应以及铝的化合物的性质来分析解答,题目难度不大.


科目:高中化学 来源: 题型:多选题
| A. | 氧化性:A2>B2>C2>D2 | B. | 还原性:C->A->B->D- | ||
| C. | 2A-+D2═2D-+A2的反应能进行 | D. | 2C-+B2═2B-+C2的反应不能进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
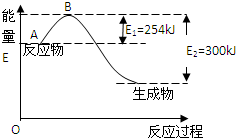 氮元素在地球上丰度较大,氮及其化合物用途广泛.请回答:
氮元素在地球上丰度较大,氮及其化合物用途广泛.请回答:| 化学键 | H-H | N≡N |
| 键能/( kJ/mol) | 435 | 943 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 萃取是常用的有机物提纯方法 | |
| B. | 燃烧法是研究确定有机物成分的有效方法之一 | |
| C. | 对有机物分子红外光谱图的研究有助于确定有机物分子中的官能团 | |
| D. | 核磁共振氢谱通常用于分析有机物的相对分子质量 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl2是氧化剂,NaOH是还原剂 | |
| B. | 被氧化的Cl原子与被还原的Cl原子的个数比为1:5 | |
| C. | 氧化剂与还原剂的物质的量的比为1:2 | |
| D. | 每生成1mol的NaClO3转移6mol的电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com