
| A. | 电解精炼铜时,粗铜与外接电源的负极相连 | |
| B. | 纯水中c(H+)=5×10-7mol•L-1,则c(OH-)=2×10-8mol•L-1 | |
| C. | CH3COONH4溶液显中性,说明CH3COONH4中的离子均不发生水解 | |
| D. | 向pH和体积均相同的盐酸和醋酸中各加入少量相同质量的锌粉,后者反应速率最大 |
分析 A.电解精炼铜时,粗铜为阳极,失去电子;
B.由水电离的氢离子与氢氧根离子相等;
C.CH3COONH4溶液显中性,可知醋酸根离子与铵根离子的水解程度相同;
D.向pH和体积均相同的盐酸和醋酸,醋酸浓度大.
解答 解:A.电解精炼铜时,粗铜为阳极,失去电子,则粗铜与外接电源的正极相连,故A错误;
B.由水电离的氢离子与氢氧根离子相等,则纯水中c(H+)=c(OH-)=5×10-7mol•L-1,故B错误;
C.CH3COONH4溶液显中性,可知醋酸根离子与铵根离子的水解程度相同,醋酸与一水合氨的电离平衡常数相同,故C错误;
D.向pH和体积均相同的盐酸和醋酸,醋酸浓度大,则各加入少量相同质量的锌粉,后者反应速率最大,故D正确;
故选D.
点评 本题考查较综合,涉及弱电解质的电离、盐类水解、电解应用,为高频考点,把握弱酸的电离、pH与浓度的关系、盐类水解与弱电解质电离的关系为解答的关键,侧重分析与应用能力的考查,注意选项B为易错点,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ | |
| B. | 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 盐酸滴在石灰石上:CO32-+2H+=CO2↑+H2O | |
| D. | 铜片插入硝酸银溶液中:Cu+2Ag+=Cu2++2Ag |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
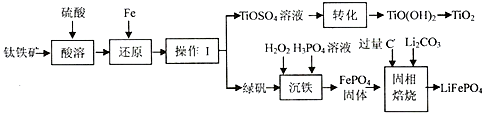
| 温度(℃) | 30 | 20 | l5 | l0 | 5 | 0 | -2 | -6 |
| FeSO4(g/L) | 240 | 190 | 130 | 117 | 95 | 79 | 59 | 38 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
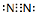 .下列能实现人工固氮的是D.
.下列能实现人工固氮的是D.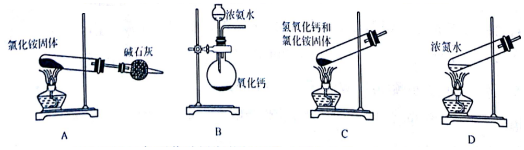
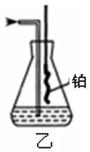
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将乙烯和乙炔气体分别通入溴的四氯化碳溶液中,两者都褪色 | |
| B. | 甲烷和氯气在室温下的光照环境中可以稳定存在 | |
| C. | 苯能使溴水褪色是因为二者反应生成了溴苯 | |
| D. | 要除去乙烷中的乙烯制得纯净的乙烷,将混合气体通入酸性高锰酸钾溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 简单离子的半径:d>c | |
| B. | 单质的沸点:a<b | |
| C. | b、d的氧化物对应的水化物均为强酸 | |
| D. | b、c可形成离子化合物b3c2 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

| Al(OH)3 | Ga(OH)3 | |
| 酸式电离常数Ka | 2×10-11 | 1×10-2 |
| 碱式电离常数Kb | 1.3×10-33 | 1.4×10-34 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 参加反应的氧化剂和还原剂的物质的量之比为3:2 | |
| B. | 被氧化和被还原的元素分别为铜和氮 | |
| C. | 当产生0.2 mol气体时,转移电子为0.6 mol | |
| D. | 被还原的CuO占参与反应CuO的$\frac{1}{2}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com