
��̼�������Ե��ܺġ�����Ⱦ�����ŷ�Ϊ�����ľ���ģʽ���Ϻ������������֮һ��ʵ�֡�������̼���ŷš���
����������ʹ���Ҵ�������Ϊ����ȼ�ϳ�������˵�̼���ã����ʵ�����ͬ���Ҵ������ͣ���ΪC8H18������ȫȼ�ղ�����CO2�����ʵ���֮��Ϊ �������ѳ���ʹ�� ��Ϊ����ȼ�Ͽ�����ʵ�֡�������̼���ŷš���
������ͣ��������װ������β���������ʩ,���ܽ�����β����CO��NOx��Ӧ���ɿɲ��������̬����ѭ���������壬д��CO��NOx��һ�������·�Ӧ�Ļ�ѧ����ʽ��
��
���������ڼ佫�ÿɽ���ġ��������ϡ����һ���Է��С����ɱ���������������֤�����ؿ���Ŀ����Ϊ�˷�ֹ������ ��Ⱦ��
��1��4������ ��2xCO+2NOx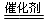 2xCO2+N2 �۰�ɫ
2xCO2+N2 �۰�ɫ
��������
�����������ȼ���Ҵ������ͺ����е�̼Ԫ����ȫת��Ϊ������̼�����ȼ����ͬ���ʵ������Ҵ�������ʱ������������̼�����ʵ���֮��Ϊ1:4.ʵ�ֶ�����̼�����ŷţ���ʹ�������Դ������
�ڷ�Ӧ�Ļ�ѧ����ʽΪ��2xCO+2NOx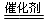 2xCO2+N2��
2xCO2+N2��
��һ�����������ڰ�ɫ��Ⱦ������á��������ϡ��ɷ�ֹ��ɫ��Ⱦ��
���㣺��̼����
��������Ҫ�����̼���õ������ѧ���������������Ƽ��Ĺ�ϵ���ѶȲ����ؿ���ѧ��������ȵ�Ĺ�ע�̶ȣ�����Ҫ����ע�⣬ƽʱҪ���ע��ѧ�������ص��ȵ����⡣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
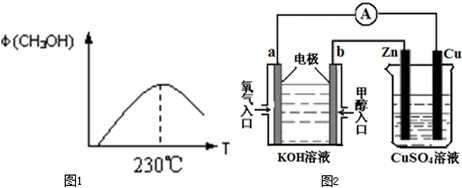
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
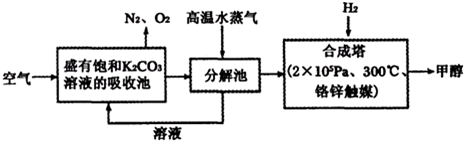
| ���� | H2 | CO | CH3OH |
| Ũ��/��mol?L-1�� | 0.2 | 0.2 | 0.4 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com