
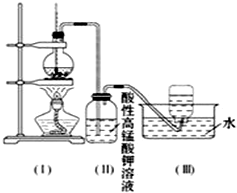
 ČēĶ¼ĖłŹ¾£¬ŌŚŹµŃéŹŅĄļ£¬Ķس£ĄūÓĆÅØĮņĖįÓėŅŅ“¼»ģŗĻ¼ÓČČÖĘŅŅĻ©£¬¼ÓČČŅ»¶ĪŹ±¼äŗóČÜŅŗÖŠÓŠŗŚÉ«ĻÖĻó³öĻÖ£®¹żŅ»¶ĪŹ±¼äŗ󣬾ĮņĖįĖį»ÆµÄøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£®¾·ÖĪöµĆÖŖ£ŗ²śÉśµÄĘųĢåÖŠŗ¬ÓŠCH2=CH2”¢SO2”¢CO2”¢H2O£®
ČēĶ¼ĖłŹ¾£¬ŌŚŹµŃéŹŅĄļ£¬Ķس£ĄūÓĆÅØĮņĖįÓėŅŅ“¼»ģŗĻ¼ÓČČÖĘŅŅĻ©£¬¼ÓČČŅ»¶ĪŹ±¼äŗóČÜŅŗÖŠÓŠŗŚÉ«ĻÖĻó³öĻÖ£®¹żŅ»¶ĪŹ±¼äŗ󣬾ĮņĖįĖį»ÆµÄøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£®¾·ÖĪöµĆÖŖ£ŗ²śÉśµÄĘųĢåÖŠŗ¬ÓŠCH2=CH2”¢SO2”¢CO2”¢H2O£®·ÖĪö £Ø1£©ŅŅ“¼ŌŚÅØĮņĖį¼ÓČČ170”ę·¢ÉśĻūČ„·“Ӧɜ³ÉŅŅĻ©ĘųĢ壻
£Ø2£©ÅØĮņĖįÓėŅŅ“¼»ģŗĻ¼ÓČČÖĘŅŅĻ©£¬¼ÓČČŅ»¶ĪŹ±¼äŗó¹Ū²ģµ½ÉÕĘæÖŠČÜŅŗ±äŗŚ£¬ĖµĆ÷ÅØĮņĖįŃõ»ÆŅŅ“¼Éś³ÉĢ¼£¬Ķ¬Ź±×ŌÉķ±»»¹Ō£¬ÖʵƵÄŅŅĻ©ĘųĢåÖŠĶس£»įŗ¬ÓŠCO2”¢SO2µČĘųĢ壬¶žŃõ»ÆĮņŗĶøßĆĢĖį¼ŲÄÜ·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬øßĆĢĖį¼ŲČÜŅŗĶŹÉ«£»
£Ø3£©ĮņĖįĖį»ÆµÄøßĆĢĖį¼ŲČÜŅŗÖŠ±¾Éķ¾Ķŗ¬ÓŠSO42-£¬ĄūÓƶžŃõ»ÆĮņ¾ßÓŠĘư׊ŌÄÜŹ¹Ę·ŗģĶŹÉ«¼ģŃ鶞Ńõ»ÆĮņ“ęŌŚ£»
£Ø4£©³żČ„¶žŃõ»ÆĮņæÉÓĆ¼īŅŗ½ųŠŠĪüŹÕ£¬ŌŚ×°ÖĆ£Ø¢ń£©ŗĶ£Ø¢ņ£©Ö®¼äŌö¼ÓĮĖŅ»øö×°ÓŠ×ćĮæĒāŃõ»ÆÄĘČÜŅŗµÄĻ“Ęų×°ÖĆ£¬ĒŅ½«£Ø¢ņ£©ĘæÖŠČÜŅŗ»»³ÉäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ£¬ŅŅĻ©Óėäåµ„ÖŹ·“Ӧɜ³É1£¬2-¶žäåŅŅĶ飮
½ā“š ½ā£ŗ£Ø1£©ŅŅ“¼ŌŚÅØĮņĖį¼ÓČČ170”ę·¢ÉśĻūČ„·“Ӧɜ³ÉŅŅĻ©ĘųĢ壬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCH3CH2OH$”ś_{170”ę}^{ÅØĮņĖį}$CH2=CH2”ü+H2O£¬
¹Ź“š°øĪŖ£ŗCH3CH2OH$”ś_{170”ę}^{ÅØĮņĖį}$CH2=CH2”ü+H2O£»
£Ø2£©ÅØĮņĖį¾ßÓŠĒæŃõ»ÆŠŌ£¬ÄÜŃõ»ÆŅŅ“¼£¬°ŃŅŅ“¼Ńõ»Æ³ÉĢ¼£¬Ķ¬Ź±×ŌÉķ±»»¹Ō³É¶žŃõ»ÆĮņ£¬¶žŃõ»ÆĮņÓėøßĆĢĖį¼Ų·“Ó¦5SO2+2KMnO4+2H2O=K2SO4+2MnSO4+2H2SO4ĶŹÉ«£¬ŅŅĻ©±»øßĆĢĖį¼ŲČÜŅŗŃõ»Æ5CH2=CH2+12KMnO+18H2SO4”ś10CO2+12MnSO4+28H2O+6K2SO4£¬µ¼ÖĀøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£»
A£®£Ø¢ņ£©ĘæÖŠĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£¬æÉÄÜŹĒ¶žŃõ»ÆĮņÓėøßĆĢĖį¼Ų·“Ó¦£¬¹ŹA“ķĪó£»
B£®£Ø¢ņ£©ĘæÖŠĖįŠŌøßĆĢĖį¼ŲČÜŅŗĶŹÉ«£¬æÉÄÜŹĒŅŅĻ©±»øßĆĢĖį¼ŲŃõ»Æ£¬¹ŹB“ķĪó£»
C£®ÄÜŹ¹øßĆĢĖį¼ŲĶŹÉ«µÄÓŠ¶žŃõ»ÆĮņŗĶŅŅĻ©£¬ĖłŅŌ²»ÄÜÖ¤Ć÷ĶØČėµÄĘųĢåŹĒ“æ¾»Īļ£¬¹ŹCÕżČ·£»
D£®ĪŽĀŪŹĒ¶žŃõ»ÆĮņ£¬»¹ŹĒŅŅĻ©£¬Ź¹øßĆĢĖį¼ŲĶŹÉ«£¬¶¼ŹĒÓėøßĆĢĖį¼Ų·¢ÉśŃõ»Æ»¹Ō·“Ó¦£¬ĒŅøßĆĢĖį¼ŲŹĒŃõ»Æ¼Į£¬ĘųĢåŹĒ»¹Ō¼Į¾ßÓŠ»¹ŌŠŌ£¬¹ŹDÕżČ·£»
¹Ź“š°øĪŖ£ŗŅŅ£»CD£»
£Ø3£©×°ÖĆ£Ø¢ņ£©ÖŠ×°ÓŠ¾ĮņĖįĖį»ÆµÄøßĆĢĖį¼ŲČÜŅŗ£¬Ėį»ÆŅżČėĮņĖįøłĄė×Ó£¬¼ÓČėŃĪĖįŗĶĀČ»Æ±µČÜŅŗ£¬²śÉś°×É«³Įµķ£¬²»ÄÜĖµĆ÷ŹĒ¶žŃõ»ÆĮņ±»øßĆĢĖį¼ŲŃõ»ÆĖłµĆ£¬øĽųŹµŃé·½°øÖ¤Ć÷ŅŅĻ©ÖŠŹĒ·ńŗ¬ÓŠSO2£¬æÉŅŌÓƶžŃõ»ÆĮņ¾ßÓŠĘư׊Ō£¬ÄÜŹ¹Ę·ŗģĶŹÉ«½ųŠŠ¼ģŃ飬·½·ØŹĒ½«£Ø¢ņ£©ĘæÖŠČÜŅŗ»»³ÉĘ·ŗģČÜŅŗ£¬
¹Ź“š°øĪŖ£ŗ²»æÉæ棻ĮņĖįĖį»ÆµÄøßĆĢĖį¼ŲČÜŅŗÖŠ±¾Éķ¾Ķŗ¬ÓŠSO42-£»
£Ø4£©¶žŃõ»ÆĮņÄÜŗĶĒāŃõ»ÆÄĘ·“Ӧɜ³ÉŃĪŗĶĖ®£¬ŅŅĻ©ŗĶĒāŃõ»ÆÄĘ²»·“Ó¦£¬ŌŚ×°ÖĆ£Ø¢ń£©ŗĶ£Ø¢ņ£©Ö®¼äŌö¼ÓĮĖŅ»øö×°ÓŠ×ćĮæĒāŃõ»ÆÄĘČÜŅŗµÄĻ“Ęų×°ÖĆ£¬æɳżČ„ŅŅĻ©ÖŠµÄ¶žŃõ»ÆĮņ£¬½«×°ÖĆ£ØII£©»»³ÉŹ¢ÓŠBr2µÄCCl4ČÜŅŗµÄĻ“ĘųĘæ»ņŹŌ¹Ü£¬äåĖ®»įĶŹÉ«£¬ŅŅĻ©ŗĶäåĖ®·¢ÉśĮĖ¼Ó³É·“Ó¦£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ£ŗCH2=CH2+Br2”śCH2BrCH2Br£¬
¹Ź“š°øĪŖ£ŗNaOHČÜŅŗ£»äåµÄĖÄĀČ»ÆĢ¼ČÜŅŗ»ņäåĖ®£»CH2=CH2+Br2”śCH2BrCH2Br£®
µćĘĄ ±¾Ģāæ¼²éĮĖŹµŃéŹŅÖĘŅŅĻ©·Ø²śĪļµÄ¼ģŃ飬ÕĘĪÕĻą¹ŲĪļÖŹµÄ»ł±¾»ÆѧŠŌÖŹŹĒ½ā“š±¾ĢāµÄ¹Ų¼ü£¬£Ø3£©ĮņĖįøłĄė×ӵļģŃéŹĒøĆĢāµÄŅדķµć£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | 0.1 mol/L NH4HCO3ČÜŅŗÖŠ£ŗK+”¢Na+”¢NO3-”¢Cl- | |
| B£® | $\frac{{k}_{W}}{c£Ø{H}^{+}£©}$=1”Į10-13 mol/LµÄČÜŅŗÖŠ£ŗNH4+”¢Na+”¢SiO32-”¢Cl- | |
| C£® | ÓėAl·“Ó¦ÄܷųöH2µÄČÜŅŗÖŠ£ŗFe2+”¢K+”¢NO3-”¢SO42- | |
| D£® | Ė®µēĄėµÄc£ØH+£©=1”Į10-13mol/LµÄČÜŅŗÖŠ£ŗK+”¢Na+”¢AlO2-”¢CO32- |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
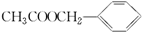 £©ŹĒĘäÖŠµÄŅ»ÖÖ£¬ĖüæÉŅŌ“ÓÜŌĄņ»ØÖŠĢįČ”£¬Ņ²æÉŅŌÓĆ¼×±½ŗĶŅŅ“¼ĪŖŌĮĻ½ųŠŠČĖ¹¤ŗĻ³É£®Ņ»ÖÖŗĻ³ÉĀ·ĻßČēĻĀ£ŗ
£©ŹĒĘäÖŠµÄŅ»ÖÖ£¬ĖüæÉŅŌ“ÓÜŌĄņ»ØÖŠĢįČ”£¬Ņ²æÉŅŌÓĆ¼×±½ŗĶŅŅ“¼ĪŖŌĮĻ½ųŠŠČĖ¹¤ŗĻ³É£®Ņ»ÖÖŗĻ³ÉĀ·ĻßČēĻĀ£ŗ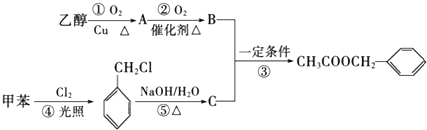
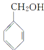 £¬BÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒōČ»ł£®
£¬BÖŠŗ¬Ńõ¹ŁÄÜĶŵÄĆū³ĘŹĒōČ»ł£®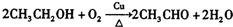 £»
£» £®
£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
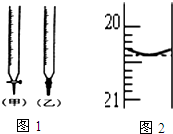 ijŠ£»ÆѧŠĖȤŠ”×é²ÉÓĆĖį¼īÖŠŗĶµĪ¶Ø·ØÓĆ0.1000mol/LNaOHČÜŅŗµĪ¶Ø“ż²āŃĪĖįČÜŅŗ£¬ŹŌ»Ų“šĻĀĆęµÄĪŹĢā£ŗ
ijŠ£»ÆѧŠĖȤŠ”×é²ÉÓĆĖį¼īÖŠŗĶµĪ¶Ø·ØÓĆ0.1000mol/LNaOHČÜŅŗµĪ¶Ø“ż²āŃĪĖįČÜŅŗ£¬ŹŌ»Ų“šĻĀĆęµÄĪŹĢā£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
 ŅŅ¶žĖįĖ×Ćū²ŻĖį£¬ĻĀĆęŹĒ»ÆѧѧĻ°Š”×éµÄĶ¬Ń§¶Ō²ŻĖį¾§Ģå£ØH2C2O4•xH2O£©½ųŠŠµÄĢ½¾æŠŌѧĻ°µÄ¹ż³Ģ£¬ĒėÄć²ĪÓė²¢ŠÖśĖūĆĒĶź³ÉĻą¹ŲѧĻ°ČĪĪń£®øĆ×éĶ¬Ń§µÄŃŠ¾ææĪĢāŹĒ£ŗĢ½¾æ²ā¶Ø²ŻĖį¾§Ģå£ØH2C2O4•xH2O£©ÖŠxÖµ£®Ķعż²éŌÄ׏ĮĻŗĶĶųĀē²éŃ°µĆ£¬²ŻĖįŅ×ČÜÓŚĖ®£¬Ė®ČÜŅŗæÉŅŌÓĆĖįŠŌKMnO4ČÜŅŗ½ųŠŠµĪ¶Ø£ŗ2MnO${\;}_{4}^{-}$+5H2C2O4+6H+ØT=2Mn2++10CO2”ü+8H2OѧĻ°Š”×éµÄĶ¬Ń§Éč¼ĘĮĖµĪ¶ØµÄ·½·Ø²ā¶ØxÖµ£®
ŅŅ¶žĖįĖ×Ćū²ŻĖį£¬ĻĀĆęŹĒ»ÆѧѧĻ°Š”×éµÄĶ¬Ń§¶Ō²ŻĖį¾§Ģå£ØH2C2O4•xH2O£©½ųŠŠµÄĢ½¾æŠŌѧĻ°µÄ¹ż³Ģ£¬ĒėÄć²ĪÓė²¢ŠÖśĖūĆĒĶź³ÉĻą¹ŲѧĻ°ČĪĪń£®øĆ×éĶ¬Ń§µÄŃŠ¾ææĪĢāŹĒ£ŗĢ½¾æ²ā¶Ø²ŻĖį¾§Ģå£ØH2C2O4•xH2O£©ÖŠxÖµ£®Ķعż²éŌÄ׏ĮĻŗĶĶųĀē²éŃ°µĆ£¬²ŻĖįŅ×ČÜÓŚĖ®£¬Ė®ČÜŅŗæÉŅŌÓĆĖįŠŌKMnO4ČÜŅŗ½ųŠŠµĪ¶Ø£ŗ2MnO${\;}_{4}^{-}$+5H2C2O4+6H+ØT=2Mn2++10CO2”ü+8H2OѧĻ°Š”×éµÄĶ¬Ń§Éč¼ĘĮĖµĪ¶ØµÄ·½·Ø²ā¶ØxÖµ£®²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗĢīæÕĢā
| ŠņŗÅ | CaCO3/mol | CaO/mol | CO2/mol |
| A | 0.02 | 0.02 | 0.05 |
| B | 0.02 | 0.02 | 0.03 |
| C | 0.02 | 0.02 | 0.01 |
| D | 0.02 | 0 | 0.05 |
| E | 0.02 | 0.02 | 0 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŹµŃéĢā
| “ĪŹż | µĪ¶ØĒ°¶ĮŹż/mL | µĪ¶Øŗó¶ĮŹż/mL |
| µŚ1“Ī | 0.00 | 1.98 |
| µŚ2“Ī | 1.98 | 4.00 |
| µŚ3“Ī | 4.00 | 5.80 |
| µŚ4“Ī | 5.80 | 7.80 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com