
 Si+2CO↑
Si+2CO↑ Si+2CO↑。
Si+2CO↑。

 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案科目:高中化学 来源:不详 题型:单选题
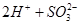 ===
===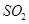 ↑
↑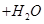 的化学反应式共有
的化学反应式共有| A.6个 | B.8个 | C.9个 | D.12个 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.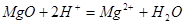 | B.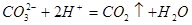 |
C.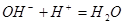 | D.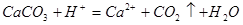 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.溴乙烷中滴入AgNO3溶液检验其中的溴元素:Br-+Ag+==AgBr↓ |
| B.用醋酸除去水垢:CaCO3 + 2H+==Ca2+ + H2O + CO2↑ |
| C.利用腐蚀法制作印刷线路板:2Fe3+ + Cu ="=" 2Fe2+ + Cu2+ |
D.AgNO3溶液中加入过量氨水: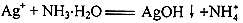 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.NaOH和Ba(OH)2组成的混合溶液中通入少量CO2:2OH-+CO2=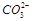 +H2O +H2O |
B.在酸性条件下,KIO3溶液与KI溶液发生反应生成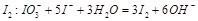 |
C.将少量亚硫酸钠溶液滴入双氧水中: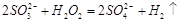 |
D.蓝色的淀粉溶液中通入足通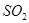 后变成无色溶液: 后变成无色溶液: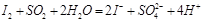 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.H2SO4与Ba(OH)2溶液反应:H++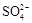 +Ba2++OH-═BaSO4↓+H2O +Ba2++OH-═BaSO4↓+H2O |
B.Ca(HCO3)2与过量Ca(OH)2溶液反应:Ca2++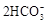 +2OH-═CaCO3↓+ +2OH-═CaCO3↓+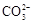 +2H2O +2H2O |
C.向Na2CO3溶液中通入少量CO2: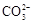 +CO2+H2O═ +CO2+H2O═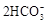 |
| D.CH3COOH溶液与NaOH溶液反应:H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用Pt电极电解少量的MgC12溶液:2H2O+2Cl-通电H2↑+C12↑+2OH- |
| B.等物质的量的Ba(OH)2与(NH4)2Fe(SO4)2在溶液中反应: Ba2++2OH-+2NH4++SO42-=BaSO4↓+2 NH3·H2O |
| C.将Na2O2固体投入H218O:2H218O+2 Na2O2=4OH-+4Na++18O2↑ |
| D.向含有0.4 mol FeBr2的溶液中通入0.3 mol Cl2充分反应: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.浓烧碱溶液中加入铝片:Al + 2OH-=AlO2-+H2↑ |
| B.向明矾溶液中滴加Ba(OH)2溶液,使SO42-全部沉淀: 2Al3+ + 6OH- +3SO42- +3Ba2+ = 2Al(OH)3↓+ 3BaSO4↓ |
| C.在2mol/L FeBr2溶液80mL中通入4.48L氯气(标况下),充分反应: 4Fe2+ +6Br- +5Cl2 = 4Fe3+ + 3Br2 + 10Cl- |
| D.用惰性电极电解饱和氯化钠溶液:2Cl- + 2H+ ==H2↑+ Cl2↑ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com