
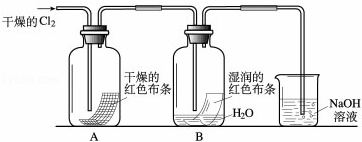
为了探究HClO的漂白性,某同学设计了如下的实验.
(1)通入Cl2后,从集气瓶A中干燥的红色布条的现象可得出的结论是 ;从集气瓶B中湿润的红色布条的现象可得出的结论是 .
(2)为了确证是HClO使湿润的红色布条褪色,你认为还应增加的实验是 .
(3)烧杯中溶液所起的作是 .
(4)为保证实验安全,当氯气以每分钟1.12L(标准状况)的流速匀速通入时,若实验需耗时4分钟,小烧杯中盛2mol•L﹣1的NaOH溶液的体积至少应为多少?(写出计算过程)
考点:
探究氯水、氯气的漂白作用.
专题:
卤族元素.
分析:
(1)氯气能使湿润的有色布条褪色,但是不能使干燥的有色布条褪色,因为氯气与水反应会生成次氯酸和盐酸,次氯酸具有漂白性,氯气没有漂白性;
(2)根据氯气和水反应的产物是盐酸和次氯酸,为了证明次氯酸的漂白性还需要证明盐酸不能使有色布条褪色;
(3)氯气有毒,可以用氢氧化钠来吸收;
(4)根据氯气和氢氧化钠反应的方程式可以求得所需氢氧化钠的体积.
解答:
解:(1)氯气不能使干燥的有色布条褪色,干燥的氯气没有漂白性,氯气能使湿润的有色布条褪色,因为氯气和水反应生成的次氯酸具有漂白性,
故答案为:干燥的氯气没有漂白性;氯水具有漂白性;
(2)氯气和水反应的产物是盐酸和次氯酸,要证明谁有漂白性,得做两个实验:证明盐酸是否有漂白性和证明次氯酸是否有漂白性的实验,故答案为:证明盐酸是否有漂白性;
(3)氯气有毒,会造成空气污染,可以用氢氧化钠来吸收,反应生成氯化钠、次氯酸钠和水,
故答案为:吸收多余的氯气;
(4)4分钟时n(Cl2)=0.2mol,根据反应方程式Cl2+2HaOH=NaCl+NaClO+H2O可知,
需要n(NaOH)=0.4mol,
所以V(NaOH)= =0.2L=200mL,
=0.2L=200mL,
答:NaOH溶液的体积至少应为200mL.
点评:
本题通过对HClO的漂白性的探究,考查学生灵活运用知识的能力和严密的化学逻辑思维能力及相关基本计算能力,题目难度虽然不大,但也具有一定的综合性,在答题时要注意规范的语言表达.


 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案 黄冈360度定制密卷系列答案
黄冈360度定制密卷系列答案 阳光考场单元测试卷系列答案
阳光考场单元测试卷系列答案科目:高中化学 来源: 题型:
W、M、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W的一种核素在考古时常用来鉴定一些文物的年代;M的氧化物是导致酸雨的主要物质之一。X的某一种单质在高空大气层中保护人类免遭太阳光中紫外线强烈侵袭;Y的基态原子核外有6个原子轨道处于半充满状态;Z能形成红色的Z2O和黑色的ZO两种氧化物。
(1)Y3+基态的电子排布式可表示为 。
(2)M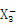 的空间构型 (用文字描述)。
的空间构型 (用文字描述)。
(3)M可形成多种氢化物,其中MH3的碱性强于M2H4的原因是_________________。
(4)根据等电子原理,WX分子的结构式为 。
(5)1 mol WX2中含有的σ键数目为 。
(6)H2X分子中X原子轨道的杂化类型为 。
(7)向Z2+的溶液中加入过量NaOH溶液,可生成Z的配位数为4的配位离子,写出该配位离子的结构式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
金属汞在加热条件下可以与氧气化合生成氧化汞,反应如下:2Hg+O2=2HgO,下列哪个选项可以说明0.3mol Hg 与0.1mol O2 充分反应后物质的种类及其量的情况?( )
|
| A. | 0.2molHgO+0.1molHg | B. | 0.2molHgO |
|
| C. | 0.2molHgO+0.1molO2 | D. | 0.1molHgO+0.1molHg |
查看答案和解析>>
科目:高中化学 来源: 题型:
在化学研究中,化学家常常先对物质进行分类,以便对同类物质的组成和性能进行深入的研究,请你将下列物质N2、HClO、CuO、KOH、NaHCO3、Fe3O4、Mg、S的正确分类填入相应的方框内:

查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述或操作不正确的是( )
|
| A. | 浓硫酸具有强氧化性,稀硫酸无氧化性 |
|
| B. | 浓硫酸不慎沾到皮肤上,立即用大量的水冲洗 |
|
| C. | 稀释浓硫酸时应将浓硫酸沿着烧杯壁慢慢地注入盛有水的烧杯中,并不断搅拌 |
|
| D. | 浓硫酸与碳的反应中,浓硫酸仅表现强氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验能证明某气体为SO2的是( )
①使澄清石灰水变浑浊
②使湿润的蓝色石蕊试纸变红
③使品红溶液褪色
④通入足量NaOH溶液中,再滴加BaCl2溶液,有白色沉淀生成,该沉淀溶于稀盐酸
⑤通入溴水中,能使溴水褪色,再滴加Ba(NO3)2溶液有白色沉淀产生.
|
| A. | 都能证明 | B. | 都不能证明 | C. | ③④⑤均能证明 | D. | 只有⑤能证明 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是( )
A. 石灰石溶于盐酸:CO32﹣+2H+═H2O+CO2↑
B. Al2O3粉末溶于NaOH溶液中:Al2O3+2OH﹣=2AlO2﹣+H2O
C. 硫酸氢钠溶液与氢氧化钡溶液的反应:Ba2++SO42﹣=BaSO4↓
D. 氧化钠加入盐酸中:O2﹣+2H+═H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com