
【题目】某矿泉水标签上印有主要的矿物质成分如下(单位为mg/L):Ca 20,K 39,Mg 3,Zn 0.06,F 0.02等,这里的 Ca,K,Mg,Zn,F是指 ( )
A. 单质 B. 元素 C. 金属离子 D. 分子
 同步学典一课多练系列答案
同步学典一课多练系列答案 经典密卷系列答案
经典密卷系列答案 金牌课堂练系列答案
金牌课堂练系列答案科目:高中化学 来源: 题型:
【题目】甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡。下列说法正确的是
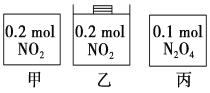
A.平衡时各容器内c(NO2)的大小顺序为乙>甲>丙
B.平衡时N2O4的百分含量:乙>甲=丙
C.平衡时甲中NO2与丙中N2O4的转化率相同
D.平衡时混合物的平均相对分子质量:甲>乙>丙
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】空气吹出法工艺,是目前“海水提溴”的最主要方法之一。其工艺流程如下:

(1)步骤③的离子方程式:_________________________________。
(2)步骤⑤中溴蒸气冷凝后得到液溴与溴水的混合物,可利用它们的相对密度相差很大的特点进行分离。分离仪器的名称是________。
(3)溴水混合物Ⅱ中溶有一定量的氯气,因此在步骤⑤中可将蒸馏产生的气体通过________(填试剂名称)溶液,以除去氯气。
(4)步骤⑤的蒸馏过程中,温度应控制在80~90 ℃。温度过高或过低都不利于生产,请解释原因:___________________________。
(5)步骤①中用硫酸酸化可提高Cl2的利用率,理由是_______________________。
(6)提取溴单质,采用蒸馏“溴水混合物Ⅱ”而不是蒸馏“溴水混合物Ⅰ”,请说明原因:
______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】据报道,意大利科学家合成了一种新型氧分子,它是由四个氧原子构成的.下列关于该分子的叙述正确的是( )
A.O2、O3、O4互为同位素
B.O2、O3、O4互为同素异形体
C.O4的摩尔质量为64
D.O2、O3、O4互称为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏伽德罗常数的值,下列叙述正确的是
A.1 L 1 mol/L FeBr2溶液与1 mol氯气反应时转移的电子数为3NA
B.0.5 mol/L硫酸钠溶液中含有溶质离子总数为1.5NA
C.1 mol硫酸氢钠固体中含阳离子总数NA
D.28 g由乙烯和聚乙烯组成的混合气体中含有碳碳双键数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,相同物质的量浓度的下列溶液:①NaCl;②NaOH;③H2SO4;④(NH4)2SO4,其中水的电离程度按由大到小顺序排列的一组是( )
A.④>③>②>① B.②>③>①>④ C.③>②>①>④ D.④>①>②>③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从银铜合金废料中回收银并制备铜化工产品的工艺如下:
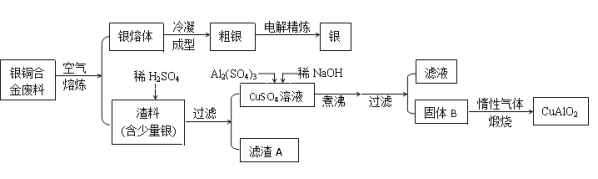
已知:①铝元素在溶液中的存在形态与溶液pH的关系如图所示。
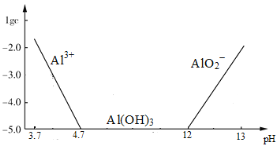
②室温时,Cu(OH)2的溶度积Ksp=2.0×10-20,当溶液中某种离子浓度小于1.0×10-5mol/L时,认为该离子沉淀完全,![]() 。
。
③Al(OH)3和Cu(OH)2开始分解的温度分别为450℃和80℃。
请回答下列问题:
(1)电解精炼银时,粗银做 极(填“阴”或“阳”),电解质选用________溶液,阴极电极反应为 。
(2)在生成固体B的过程中,需控制NaOH的加入量,使溶液的pH范围在 ,若控制不当,使NaOH过量可能会引起的反应的离子方程式为 。
(3) 煅烧过程中发生多步反应,写出最终生成CuAlO2的反应的化学方程式: 。
(4)若银铜合金中铜的质量分数为64%,理论上1.0 kg废料中的铜可完全转化为CuAlO2,至少需要1.0 mol·L-1的Al2(SO4)3溶液 L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在KNO3、MgSO4、K2SO4组成的混合溶液中Mg2+0.5 mol、NO3-0.2 mol、SO42- 0.6 mol,则溶液中K+的物质的量为( )
A.0.4 mol B.0.3 mol C.0.2 mol D.0.1 mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com