
【题目】下列说法正确的是
A.分子内共价键越强,分子越稳定,其形成的晶体的熔沸点也越高
B.离子键的本质就是阴、阳离子之间的相互吸引
C.金刚石转化为石墨的过程中不存在化学键被破坏的过程
D.由原子构成的晶体可能是原子晶体,也可能是分子晶体
科目:高中化学 来源: 题型:
【题目】工业合成氨的反应为:N2+3H2![]() 2NH3,该反应在一定条件下的密闭容器中进行。下列关于该反应的说法正确的是( )
2NH3,该反应在一定条件下的密闭容器中进行。下列关于该反应的说法正确的是( )
A. 达到平衡时,反应速率:v(正)=v(逆)=0
B. 使用催化剂可加快反应速率,提高生产效率
C. 为了提高H2的转化率,应适当增大H2的浓度
D. 若在密闭容器加入1molN2和过量的H2,最后能生成2molNH3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分解:2Mg5Al3(OH)19(H2O)4![]() 27H2O↑+10MgO+3Al2O3。
27H2O↑+10MgO+3Al2O3。
(1)用离子方程式表示除去固体产物中Al2O3的原理______________________________。
(2)已知MgO可溶于NH4Cl的水溶液,用化学方程式表示其原理__________________。
Ⅱ.NaH和NaAlH4都是重要的还原剂,一定条件下金属钠和H2反应生成NaH。NaH与水反应可生成H2,NaH与AlCl3反应可得到NaAlH4,请推测并回答:
(1)NaH与AlCl3反应得到NaAlH4的化学方程式___________________________________。
(2)NaAlH4与水发生氧化还原反应的化学方程式__________________________________。
(3)NaH在无水条件下可作为某些钢铁制品的脱锈剂(铁锈的成分表示为Fe2O3),脱锈过程中生成两种产物,其反应的化学方程式为_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列表示物质结构的化学用语正确的是 ( )
A. HF的电子式: ![]() B. HClO的结构式:H—O—Cl
B. HClO的结构式:H—O—Cl
C. S2-的结构示意图:![]() D. CaO的俗名:熟石灰
D. CaO的俗名:熟石灰
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对可逆反应A(g)+2B(g) ![]() 3C(g)的叙述中能说明已达到平衡的是( )。
3C(g)的叙述中能说明已达到平衡的是( )。
A. 混合气体的总物质的量不再变化。 B. 混合气体的总质量不再变化。
C. 容器内的压强不再变化。 D. 某一物质的物质的量不再变化。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为验证卤素单质氧化性的相对强弱,某小组用下图所示装置进行实验(夹持仪器已略去,气密性已检验)。
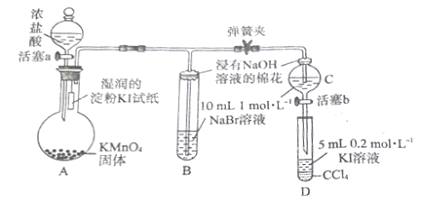
实验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸;
Il.当B和C中的溶液都变为黄色时,夹紧弹簧夹;
III.当B中溶液由黄色变为棕红色时,关闭活塞a;
IV....
(1) A中产生黄绿色气体,其化学方程式是____________________________
(2) 验证氯气的氧化性强于碘的实验现象是_____________________________
(3) B中溶液发生反应的离子方程式是______________________________
(4) 为验证溴的氧化性强于碘,过程IV的操作和现象是______________________________
(5) 过程III实验的目的是_____________________________
(6)氯、溴、碘单质的氧化性逐渐减弱的原因:同主族元素从上到下半径逐渐_______(填“增大”或“减小”),得电子能力逐渐______________(填“增强“或“减弱”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】50mL浓硫酸和铜片加热后反应,铜片完全溶解后测得产生4.48L(标况下)气体,把反应后的溶液稀释至1L,取20mL溶液加入足量BaCl2溶液产生3.262g沉淀,求原硫酸溶液的物质的量浓度是多少______?
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com