
mA(s)+nB(g)⇌qC(g)的可逆反应中,图甲在恒温条件达平衡时,B的体积分数(B%)与压强(p)的关系,图乙表示在一定条件下达到平衡(v正=v逆)后t1时刻改变影响平衡的另一个条件重新建立新平衡的反应过程,有关叙述正确的是( )
|
| A. | n<q | B. | n>q |
|
| C. | 正反应为放热反应 | D. | X点比Y点反应速率快 |
考点:
化学平衡的影响因素.
专题:
化学平衡专题.
分析:
由图象的曲线变化特征可知,增大压强,B的百分含量增大,说明平衡向逆反应方向移动,由于A为固体,则有n<q,在曲线上的点为平衡状态,以此来解答该题.
解答:
解:A、B.由图象的曲线变化特征可以看出,增大压强,B的百分含量增大,说明平衡向逆反应方向移动,由于A为固体,则有n<q,故A正确,B错误;
C.图象乙改变条件正逆反应速率都增大,逆反应速率增大的大多,平衡逆向进行,温度升高平衡逆向进行,正反应为放热反应,故C正确;
D.由图象可以看出X点的压强小于Y点压强,压强越大,反应速率越大,故X点比Y点的反应速率慢,故D错误.
故选:AC.
点评:
本题考查化学平衡曲线问题,题目难度不大,本题注意分析纵坐标随横坐标变化的趋势,特别是曲线的上的点与曲线外的点的区别.


 世纪百通期末金卷系列答案
世纪百通期末金卷系列答案科目:高中化学 来源: 题型:
向四个体积相同的密闭容器(甲、乙、丙、丁)中分别充入一定量的SO2和O2,开始反应时,按反应速率由大到小排列顺序正确的是()
甲:在500℃时,10mol SO2和6mol O2反应
乙:在500℃时,用V2O5作催化剂,10mol SO2和5mol O2反应
丙:在450℃时,8mol SO2和5mol O2反应
丁:在500℃时,8mol SO2和5mol O2反应.
A. 甲、乙、丙、丁 B. 乙、甲、丙、丁 C. 乙、甲、丁、丙 D. 丁、丙、乙、甲
查看答案和解析>>
科目:高中化学 来源: 题型:
某天然拒食素具有防御非洲大群蚯蚓的作用,其结构简式如图(未表示出原子或原子团的空间排列).该拒食素与下列某试剂充分反应,所得有机物分子的官能团数目增加,则该试剂是()
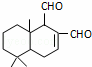
A. Br2的CCl4溶液 B. Ag(NH3)2OH溶液
C. HBr D. H2
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A有稳定性好、抗氧化能力强的特点,其结构如图 .分子中片段X对A的性能起了重要作用,为研究X的结构,将化合物A在一定条件下水解只得到B(
.分子中片段X对A的性能起了重要作用,为研究X的结构,将化合物A在一定条件下水解只得到B(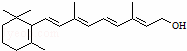 )和C.经测定确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,跟NaHCO3溶液反应有CO2产生
)和C.经测定确定C的分子式为C7H6O3,C遇FeCl3水溶液显紫色,跟NaHCO3溶液反应有CO2产生
完成下列填空:
(1)化合物B能发生下列哪种类型的反应
a.取代反应b.加成反应c.缩聚反应d.氧化反应
(2)化合物C能经下列反应得到G(分子式为C8H6O2,分子内含五元环).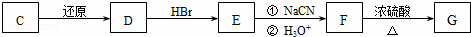
已知:ROOH RCH2OH RX
RCH2OH RX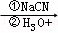 RCOOH
RCOOH
化合物C的结构简式为 .
(3)反应F→G的化学方程式为
(4)化合物E有多种同分异构体,1H核磁共振谱图表明,其中某些同分异构体含有苯环,且苯环上有两种不同化学环境的氢,写出这些同分异构体中任意三种的结构简式、、.
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应mA(g)+nB(s)⇌pC(g)+qD(g),反应过程中,其他条件不变时,产物D的物质的量分数D%与温度T或压强p的关系如图,下列说法正确的是( )
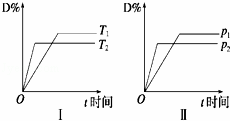
|
| A. | 化学方程式中化学计量数:m>p+q |
|
| B. | 降温可使化学平衡向正反应方向移动 |
|
| C. | 使用合适的催化剂可使D%有所增加 |
|
| D. | B的颗粒越小,正反应速率越快,有利于平衡向正反应方向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
利用“化学蒸气转移法”制备TaS2晶体,某温度下的2L恒容密闭容器中加入一定量 的 I2(g)和TaS2(s)发生如下反应:TaS2(s)+2I2(g)⇌TaI4(g)+S2(g)△H=a kJ•mol﹣1 (Ⅰ)达平衡时,TaS2(s)、I2(g)、TaI4(g)、S2(g)的物质的量分别为3mol、2mol、2mol、2mol.
(1)反应(Ⅰ)的平衡常数表达式K=
(2)若该温度下该容器中某时刻TaS2(s)、I2(g)、TaI4(g)、S2(g)的物质的量分别为2mol、2mol、4mol、4mol,则该时刻平衡向 (填“正反应”或“逆反应”)移动,v正 v逆(填“>”、“=”或“<”).
(3)在不同温度下,该反应的平衡常数K如下表:
| 温度/℃ | 40 | 80 | 200 |
| 平衡常数K | 1 | 1.5 | 4 |
该反应的△H 0(填“>”、“=”或“<”).
(4)40℃时,向该恒容密闭容器中加入2mol I2(g)和4mol TaS2(s),I2(g)的平衡转化率为 写出计算过程,结果保留小数点后1位)
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
-A.-同种胶体带同种电荷,相互排斥,是胶体稳定的主要原因
-B.-生石灰与水混合的过程只发生物理变化
-C.-O3是由3个氧原子构成的化合物
-D.-可用丁达尔效应区分溶液与胶体
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)在25℃、101kPa的条件下,同质量的CH4和A气体的体积之比是11:4,则A的摩尔质量为 .
在V L Al2(SO4)3溶液中,测得含Al3+的质量为a g,则Al2(SO4)3溶液的物质的量浓度为 mol/L,SO42﹣的物质的量浓度为 mol/L.
(3)将5.3gNa2CO3溶于水配成1L溶液,要使Na+浓度变为0.2mol/L,需要加入NaCl固体 g
(4)实验测得CO和O2混合气体的密度是氢气的15.5倍,其中氧气的体积分数为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
|
| A. | 摩尔是6.02×1023个结构微粒的集体 |
|
| B. | 0.012kg12C所含的原子数精确值是6.02×1023 |
|
| C. | 1molH就是1mol氢 |
|
| D. | 1molH2SO4的质量是98g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com