
对于在一密闭容器中进行的下列反应:
C(s)+O2(g) CO2(g),下列说法中错误的是 ( )
CO2(g),下列说法中错误的是 ( )
A.将木炭粉碎成粉末状可以加快化学反应速率
B.升高温度可以加快化学反应速率
C.增加压强可以加快化学反应速率
D.增加木炭的量可以加快化学反应速率
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
以苯酚为原料合成  的路线如下所示.请按要求作答:
的路线如下所示.请按要求作答:

(1)写出以下物质的结构简式:B ,F .
(2)写出反应④、⑤的化学反应方程式:④ ⑤
(3)反应⑤可以得到E,同时可能得到的副产物的结构简式为, .
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组同学展开对漂白剂亚氯酸钠(NaClO2)的研究。
实验Ⅰ:制取NaClO2晶体
已知:NaClO2饱和溶液在温度低于38℃时析出的晶体是NaClO2•3H2O,高于38℃时析出晶体的是NaClO2,高于60℃时NaClO2分解成NaClO3和NaCl。Ba(ClO)2可溶于水。
利用下图所示装置进行实验。
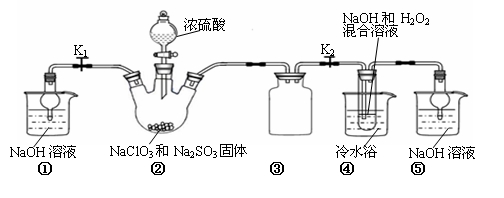
(1)装置①的作用是 装置③的作用是 。
(2)装置②中产生ClO2的化学方程式为 。
(3)从装置④反应后的溶液获得晶体NaClO2的操作步骤为:
①减压,55℃蒸发结晶;②趁热过滤;③ ;④低于60℃干燥,得到成品。
(4)设计实验检验所得NaClO2晶体是否含有杂质Na2SO4,操作与现象是:取少量晶体溶于蒸馏水, 。
实验Ⅱ:测定某亚氯酸钠样品的纯度。
设计如下实验方案,并进行实验:
①准确称取所得亚氯酸钠样品m g于烧杯中,加入适量蒸馏水和过量的碘化钾晶体,再滴入适量的稀硫酸,充分反应(已知:ClO2-+ 4I-+4H+ =2H2O+2I2+Cl-)。将所得混合液配成100mL待测溶液。
②移取25.00mL待测溶液于锥形瓶中,用c mol•L-1 Na2S2O3标准液滴定,至滴定终点。重复2次,测得消耗标准溶液的体积的平均值为V mL(已知:I2 +2S2O32-=2I-+S4O62-)。
(5)滴定中使用的指示剂是 ,达到滴定终点时的现象为 。
(6)样品中NaClO2的质量分数为 (用含m、c、V的代数式表示,式量:NaClO2 90.5)。
查看答案和解析>>
科目:高中化学 来源: 题型:
卤代烃广泛用于化工生产,下列关于卤代烃的说法正确的是( )
A.卤代烃性质稳定,不会对环境造成破坏
B.卤代烃均难溶于水
C.卤代烃都能发生消去反应
D.有小分子(如水)生成的反应是消去反应
查看答案和解析>>
科目:高中化学 来源: 题型:
设C+CO2 2CO(正反应吸热),反应速率为v1;N2+3H2
2CO(正反应吸热),反应速率为v1;N2+3H2 2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为 ( )
2NH3(正反应放热),反应速率为v2。对于上述反应,当温度升高时,v1和v2的变化情况为 ( )
A.同时增大 B.同时减小
C.v1增加,v2减小 D.v1减小,v2增大
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应M+N Q达到平衡时,下列说法正确的是 ( )
Q达到平衡时,下列说法正确的是 ( )
A.M、N、Q三种物质的浓度一定相等
B.M、N全部变成了Q
C.反应物和生成物的浓度都保持不变
D.反应已经停止
查看答案和解析>>
科目:高中化学 来源: 题型:
电浮选凝聚法是工业上采用的一种污水处理方法:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀。Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用。阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用。某科研小组用电浮选凝聚法处理污水,设计装置示意图如下:
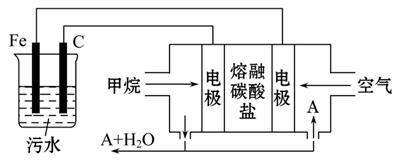
(1)实验时若污水中离子浓度较小,导电能力较差,产生气泡速率缓慢,无法使悬浮物形成浮渣。此时,应向污水中加入适量的________。
a.BaSO4 b.CH3CH2OH c.Na2SO4 d.NaOH
(2)电解池阳极发生了两个电极反应,其中一个反应生成一种无色气体,则阳极的电极反应式分别是
Ⅰ.________________________________________________________________;
Ⅱ.________________________________________________________________。
(3)电极反应Ⅰ和Ⅱ的生成物反应得到Fe(OH)3沉淀的离子方程式是________
__________________________________________________________。
(4)该燃料电池是以熔融碳酸盐为电解质,CH4为燃料,空气为氧化剂,稀土金属材料作电极。为了使该燃料电池长时间稳定运行,电池的电解质组成应保持稳定,电池工作时必须有部分A物质参加循环(见上图)。A物质的化学式是___
___________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、R是短周期主族元素,X原子最外层电子数是次外层的两倍,Y元素在地壳中的含量最多,Z元素的化合物的焰色反应呈黄色,R原子的核外电子数是X原子与Z原子的核外电子数之和。下列叙述正确的是 ( )
A.X与Y能形成两种常见的气态化合物
B.原子半径的大小顺序:r(X)>r(Y)>r(Z)>r(R)
C.X、Z分别与R形成的化合物中化学键类型不同
D.含有Y、Z、R三种元素的化合物最多只有2种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com