
| 选项 | A | B | C | D |
| 实验 目的 | 除去KCl中少量MnO2 | 用10mol•L-1盐酸配制100mL 0.1mol•L-1盐酸 | 用含有少量NH4Cl杂质的NaCl溶液制备氯化钠晶体 | 除去乙烯中少量SO2 |
| 实验仪器或装置 | 烧杯、玻璃棒、分液漏斗 | 100mL容量瓶、玻璃棒、烧杯 |  |  |
| A. | A | B. | B | C. | C | D. | D |
分析 A.除去氯化钾中的二氧化锰,需要通过过量操作完成,不属于分液漏斗;
B.配制一定物质的量浓度的溶液时,必须使用胶头滴管、量筒;
C.氯化铵不稳定,可通过加热的方法除去氯化钠中的杂质氯化铵;
D.乙烯和二氧化硫都能够与酸性高锰酸钾溶液反应.
解答 解:A.MnO2难溶于水,KCl易溶于水,故采用溶解、过滤的方法,应该用普通漏斗而不是分液漏斗,故A错误;
B.用10mol•L-1盐酸配制100mL 0.1mol•L-1盐酸,缺少量取盐酸的仪器,如酸式滴定管或量筒,故B错误;
C.用含有少量NH4Cl杂质的NaCl溶液制备氯化钠晶体,由于氯化铵不稳定,加热易分解,则可以通过蒸发操作完成,故C正确;
D.二氧化硫和乙烯均能与酸性KMnO4溶液反应,故不能达到除杂的目的,故D错误;
故选C.
点评 本题考查化学实验方案的设计与评价,题目难度不大,侧重考查化学实验基本操作方法,意在考查考生对化学实验操作中所需的仪器、原理的分析能力.


 状元坊全程突破导练测系列答案
状元坊全程突破导练测系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ②③⑤⑥ | C. | ①④⑤⑥ | D. | ①③④⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 ,下列有关M性质的叙述中错误的是( )
,下列有关M性质的叙述中错误的是( )| A. | M与金属钠完全反应时,二者物质的量之比为1:2 | |
| B. | M与碳酸氢钠完全反应时,二者物质的量之比为1:1 | |
| C. | M与氢氧化钠完全反应时,二者物质的量之比为1:2 | |
| D. | M既能与乙酸反应,又能与乙醇反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 金属阳离子的半径大于它的原子半径 | |
| B. | 金属阳离子的半径小于它的原子半径 | |
| C. | 非金属阴离子的半径小于其原子半径 | |
| D. | 核外电子排布相同的不同微粒,核电荷数越大半径越小 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 高氯酸(HClO4)的酸性比硫酸强 | B. | 次氯酸的氧化性比稀硫酸强 | ||
| C. | 氯化氢比硫化氢的热稳定性好 | D. | 硫离子还原性比氯离子还原性强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①② | B. | ①④ | C. | ②③ | D. | ③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A可发生如图所示的一系列化学反应.据图回答下列问题:
某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家的石油化工发展水平,A可发生如图所示的一系列化学反应.据图回答下列问题: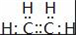 ,D中官能团的名称是羟基.
,D中官能团的名称是羟基.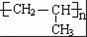 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com