
| A. | 氢气 | B. | 氧气 | C. | 氮气 | D. | 二氧化碳 |
科目:高中化学 来源: 题型:选择题
| A. | 粗铜板作阳极,纯铜片作阴极,CuSO4溶液作电解液 | |
| B. | 电解时,阳极发生氧化反应,而阴极发生的反应为:Cu2++2e-═Cu | |
| C. | 粗铜中所含Ni、Fe、Zn等金属杂质,电解后以单质形式沉积槽底,形成阳极泥 | |
| D. | 电解铜的纯度可达99.95%~99.98% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 肥肉中的油脂 | B. | 谷类中的淀粉 | C. | 蔬菜中的纤维素 | D. | 瘦肉中的蛋白质 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NH4CuSO3中只有Cu元素被氧化 | |
| B. | 反应中硫酸作氧化剂 | |
| C. | 刺激性气味的气体是二氧化硫 | |
| D. | 1 mol NH4CuSO3完全反应转移0.5 mol电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
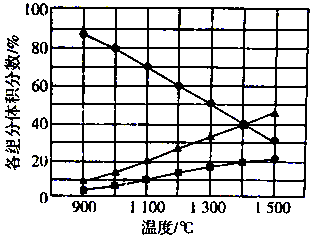 H2S在高温下分解生成硫蒸气(S2)和H2,不同温度下,反应体系中各组分的体积分数如图所示.则1400℃时反应体系中混合气体的平均摩尔质量为( )
H2S在高温下分解生成硫蒸气(S2)和H2,不同温度下,反应体系中各组分的体积分数如图所示.则1400℃时反应体系中混合气体的平均摩尔质量为( )| A. | 20.8g/mol | B. | 27.2 g/mol | C. | 33.3 g/mol | D. | 39.6 g/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有电子转移是氧化还原反应的本质,有元素化合价的变化是氧化还原反应的外在表现 | |
| B. | 一种物质被氧化,必然有另一种物质被还原 | |
| C. | 被氧化的物质得到或偏向电子,被还原的物质失去或偏离电子 | |
| D. | 氧化反应就是得到或偏向电子的反应,还原反应就是失去或偏离电子的反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸钙溶于稀盐酸中:CaCO3+2H+═Ca2++H2O+CO2↑ | |
| B. | 少量的金属铜加入到FeCl3溶液中:Fe3++Cu═Fe2++Cu2+ | |
| C. | 铝粉投入到NaOH溶液中:2Al+2OH-═2AlO2-+H2↑ | |
| D. | 将少量NaOH溶液与足量Ba(HCO3)2溶液混合:Ba2++2HCO3-+2OH-═BaCO3↓+2H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验目的 | 操作 | |
| A | 检验淀粉水解产物有还原性 | 淀粉溶液和稀H2SO4混合加热,冷却后,再加新制的Cu(OH)2悬浊液加热至沸腾 |
| B | 证明SO2具有漂白性 | 将SO2通入溴水中 |
| C | 为了提取溴水中的溴 | 加入植物油进行萃取 |
| D | 浓、稀HNO3分别与Cu反应 | 比较浓、稀HNO3的氧化性强弱 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com