
| m(CO)+m(H2) |
| n(CO)+n(H2) |
| 28n(CO)+2n(H2) |
| n(CO)+n(H2) |
| n(CO) |
| n(H2) |
| 5 |
| 8 |
| 5 |
| 8 |


 ��1����Ԫ�¿�������ĩϵ�д�
��1����Ԫ�¿�������ĩϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A�����³�ѹ��28��N2������ԭ����ĿΪ2NA |
| B����״����0.5molH2O���е�ԭ����ĿΪ1.5NA |
| C���κ�������0.5mol�������ӵķ�����һ����0.5NA |
| D��49��H2SO4�к��е�ԭ����ĿΪ1.5NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
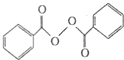 ����ȥ���������������������Ŀǰ�ѱ����ã�
����ȥ���������������������Ŀǰ�ѱ����ã�
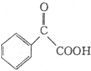 �����̣�ʾ�����£�
�����̣�ʾ�����£�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ܢ� | B���٢� | C���ڢۢ� | D���ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1 mol?L-1 ��NH4��2Fe��SO4��2��Һ��c��SO42-����c��NH4+����c��Fe2+����c��H+�� |
| B��0.1 mol?L-1 NaHCO3��Һ��c��Na+��+c��H+��=c��CO32-��+c��HCO3-��+c��OH-�� |
| C��0.1 mol?L-1Na2S��Һ��2c��Na+��=c��S2-��+c��HS-��+c��H2S�� |
| D��0.01 mol?L-1NaOH��Һ������pH=2�Ĵ����Ϻ����Һ��c ��CH3COO-����c ��Na+����c ��H+����c ��OH-�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���������Һ�м���������ˮ������Һ��pH=7ʱ��c��SO42-����c��NH4+�� |
| B�������£������ʵ���Ũ�ȵ� ��NH4��2CO3 ��Na2CO3��Һ��ǰ�ߵ�c��HCO3-��С |
| C��NaHCO3��Һ������Ũ�������¹�ϵ��c��CO32-��+c ��OH-��=c ��H+��+c��H2CO3�� |
| D�������ʵ���Ũ�ȡ��������NaX������HX��Һ��Ϻ�����Ũ�ȹ�ϵ�ǣ�c��Na+����c��HX����c��X-����c��OH-����c��H+�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| ʱ�䣨min�� Ũ�ȣ�mol��L-1�� ʵ�����/�¶ȣ��棩 | 0 | 10 | 20 | 30 | 40 | 50 |
| ʵ��1/800 | 1.00 | 0.80 | 0.65 | 0.55 | 0.50 | 0.50 |
| ʵ��2/800 | 1.00 | 0.70 | 0.50 | 0.50 | 0.50 | 0.50 |
| ʵ��3/800 | 1.00 | 0.50 | 0.40 | 0.15 | 0.15 | 0.15 |
| A��ʵ��2��ʵ��1�ķ�Ӧ������ѹǿ��С |
| B��ʵ��2��ʵ��lʹ����Ч�ʸ��ߵĴ��� |
| C��ʵ��1��ʵ��3��ƽ�ⳣ���� |
| D��ʵ��2��ʵ��3���жϸ÷�Ӧ�Ƿ��ȷ�Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���ζ�ʱ�����ֿ��Ƶζ��ܻ����������ճ���ƿ���ߵα����۾�ע�ӵζ����е�Һ�� |
| B���ⶨij��ɫ��Һ��pHֵʱ���ø���Ľྻ������պȡ��Һ������pH��ֽ�ϣ�������ɫ���Ƚ� |
| C���ζ���ϴ��������ˮ��ϴ������ע���Һ���еζ� |
| D����ij����Һ�м����������Ʋ����ȣ���ʪ�����ɫʯ����ֽ��������죬˵��ԭ��Һ��NH4+ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com