
用NA表示阿伏加德罗常数的值.下列叙述正确的是( )
|
| A. | 常温常压下,1mol C2H4所含的电子数为12NA |
|
| B. | 标准状况下,16g甲烷中共价键数目为4NA |
|
| C. | 常温常压,4 g氦气所含的核外电子数为4NA |
|
| D. | 16g氧气和臭氧的混合物中含有1.5NA个氧原子 |
考点:
阿伏加德罗常数.
专题:
阿伏加德罗常数和阿伏加德罗定律.
分析:
A.乙烯分子中含有16mol电子,1mol乙烯中含有16mol电子;
B.甲烷分子中含有4个碳氢共价键,16g甲烷的物质的量为1mol,含有4mol共价键;
C.稀有气体为单原子分子,4g氦气的物质的量为1mol,含有2mol电子;
D.氧气和臭氧都只含有氧元素,16g二者的混合物中含有16g氧原子,含有1mol氧原子.
解答:
解:A.1mol乙烯中含有16mol电子,4所含的电子数为16NA,故A错误;
B.16g甲烷的物质的量为1mol,1mol甲烷中含有4mol碳氢键,含有的共价键数目为4NA,故B正确;
C.4g氦气的物质的量为1mol,1mol氦气中含有1mol氦原子,含有2mol电子,所含的核外电子数为2NA,故C错误;
D.16g氧气和臭氧的混合物中含有16g氧原子,含有氧原子的物质的量为1mol,含有NA个氧原子,故D错误;
故选B.
点评:
本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,准确弄清分子、原子、原子核内质子中子及核外电子的构成关系.


科目:高中化学 来源: 题型:
1996年诺贝尔化学奖授予斯莫利等三位化学家,以表彰他们发现富勒烯(C60)开辟了化学研究的新领域.后来,人们又发现了一种含碳量极高的链式炔烃──棒碳,它是分子中含300~500个碳原子的新物质,其分子中只含有交替连接的单键和叁键.对于C60与棒碳,下列说法正确的是( )
|
| A. | C60与棒碳中所有的化学键都是非极性共价键 |
|
| B. | 棒碳不能使溴水褪色 |
|
| C. | C60在一定条件下可能与CuO发生置换反应 |
|
| D. | 棒碳与乙炔互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图所示,下列表述正确的是( )

A.反应的化学方程式为:2MN
B.t2时,正、逆反应速率相等,达到平衡
C.t3时,正反应速率大于逆反应速率
D.t1时,N的浓度是M浓度的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
在重水D2O中存在电离:D2O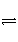
 D++OD-,因此,对D2O可以采用同pH一样的定义来规定pD,即pD=-lg[D+]。已知在某温度下,D2O达电离平衡时,[D+][OD-]=1.6×10-15 mol2·L-2,则纯净的D2O在此温度下的pD________7(填“>”、“<”或“=”)。此温度下,若用0.01 mol DCl溶于D2O配成1 L溶液,pD________;若用0.01 mol NaOD溶于D2O配成1 L溶液时,pD________12(填“>”、“<”或“=”)。
D++OD-,因此,对D2O可以采用同pH一样的定义来规定pD,即pD=-lg[D+]。已知在某温度下,D2O达电离平衡时,[D+][OD-]=1.6×10-15 mol2·L-2,则纯净的D2O在此温度下的pD________7(填“>”、“<”或“=”)。此温度下,若用0.01 mol DCl溶于D2O配成1 L溶液,pD________;若用0.01 mol NaOD溶于D2O配成1 L溶液时,pD________12(填“>”、“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是( )
|
| A. | ⅠA族元素单质的熔点从上往下逐渐降低 |
|
| B. | 分子晶体中一定存在共价键 |
|
| C. | ⅥA族元素的氢化物中,稳定性最好的其沸点也最高 |
|
| D. | 同周期非金属氧化物对应的水化物的酸性从左往右依次增强 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知铍(Be)的原子序数为4.下列对铍及其化合物的叙述中,正确的是( )
|
| A. | 铍的原子半径小于硼的原子半径 |
|
| B. | 氧化铍分子中铍原子的最外层电子数是8 |
|
| C. | 氢氧化铍的碱性比氢氧化钙的弱 |
|
| D. | 单质铍跟冷水反应产生氢气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有NaBr、KI的溶液中通入过量的Cl2,然后将溶液蒸干,并灼烧固体,最后得到的物质是( )
|
| A. | KCl | B. | NaCl和KCl | C. | NaCl和KBr | D. | NaCl、KCl和I2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知H2(g)+Cl2(g)═2HCl(g)△H=﹣184.6kJ/mol,则反应HCl(g)═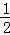 H2(g)+
H2(g)+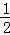 Cl2(g)的△H为( )
Cl2(g)的△H为( )
|
| A. | +184.6kJ/mol | B. | ﹣92.3kJ/mol | C. | ﹣369.2kJ/mol | D. | +92.3kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com