
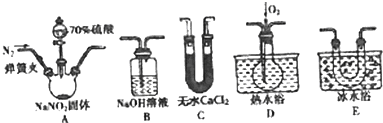
分析 (1)根据各部分装置的作用进行连接,C吸收水蒸气,B尾气处理,防止污染空气,D检验NO,E冷却二氧化氮;
(2)NO很容易被氧气氧化,装置中有空气,无法检验有NO生成;
(3)①依据图象和作用判断盛浓硫酸的仪器;
②根据一氧化氮和氧气反应生成红棕色二氧化氮气体判断,温度低于二氧化氮液化温度时,二氧化氮变成液态;
(4)根据反应物和生成物写出反应方程式,该反应中生成二氧化氮、一氧化氮,同时还有硫酸钠、水生成.
解答 解:(1)C吸收水蒸气,B尾气处理,防止污染空气,D检验NO,E冷却二氧化氮,利用D检验NO,所以装置的连接为A→C→E→D→B,故答案为:ACEDB;
(2)NO很容易被氧气氧化,装置中有空气,无法检验有NO生成,所以通氮气的目的是排尽整个装置中的空气,防止产生的NO被氧化生成NO2,
故答案为:防止可能生成的NO被完全氧化成NO2,造成对A中反应气体产物检验的干扰;
(3)①盛装70%浓硫酸的仪器名称是分液漏斗,
故答案为:分液漏斗;
②D中刚开始为无色,通入O2后变为红棕色,D中无色气体变成红色,说明含有NO气体,
故答案为:D中刚开始为无色,通入O2后变为红棕色;
(4)通过以上分析知,该反应中生成二氧化氮、一氧化氮,同时还有硫酸钠、水生成,所以反应方程式为2NaNO2+H2SO4=Na2SO4+NO2↑+NO↑+H2O,
故答案为:2NaNO2+H2SO4=Na2SO4+NO2↑+NO↑+H2O.
点评 本题考查实验方案设计,明确物质的性质和实验原理是解本题关键,注意实验设计要遵循严密性、可行性、科学性的原则,题目难度中等.


科目:高中化学 来源: 题型:多选题
| A. | 3s2和3s23p5 | B. | 2s22p2和2s22p4 | C. | 1s1和3s23p4 | D. | 3s23p4和2s22p4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
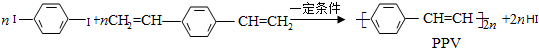
| A. | PPV是聚苯乙炔 | |
| B. | 该反应为缩聚反应 | |
| C. | PPV与聚苯乙烯的最小结构单元组成相同 | |
| D. | 1 mol 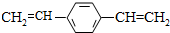 最多可与2 mol H2发生反应 最多可与2 mol H2发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
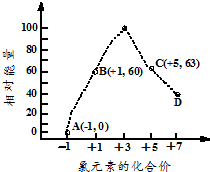
| A. | 含氧酸的酸性:H3ZO4>H2YO4>HXO4 | |
| B. | 原子半径:Z>Y>X | |
| C. | 气态氢化物的稳定性按X、Y、Z顺序由弱到强 | |
| D. | 元素的负化合价的绝对值按X、Y、Z顺序由小到大 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,X属于共价化合物.
,X属于共价化合物. .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 填写下列空白:
填写下列空白: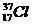 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
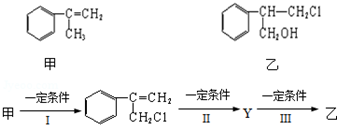
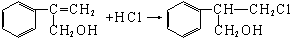 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com