
【题目】下列物质中,能作为制备木材防火剂原料的是
A. 水玻璃 B. 氢氟酸 C. “84”消毒液 D. 硫酸钠溶液
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z分别为原子序数递增的短周期元素,X、Y的阳离子与Ne具有相同的电子层结构, 且其单质均可与冷水反应,生成W的单质;Z的单质为黄绿色气体。下列说法正确的是
A. W与X形成的简单二元化合物的电子式为![]()
B. 短周期元素中Y的原子半径最大
C. 工业上通过电解Y的氧化物制取Y的单质
D. 最外层电子数等于其电子层数的金属与Z形成离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三个密闭容器中分别充入N2、H2、O2三种气体,以下各种情况下排序正确的是
A.当它们的温度和压强均相同时,三种气体的密度:ρ(H2)>ρ(N2)>ρ(O2)
B.当它们的温度和密度都相同时,三种气体的压强:p(H2)>p(N2)>p(O2)
C.当它们的质量和温度、压强均相同时,三种气体的体积:V(O2)>V(N2)>V(H2)
D.当它们的压强和体积、温度均相同时,三种气体的质量:m(H2)>m(N2)>m(O2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工生产要遵守三大原则:充分利用原料、充分利用能量、保护环境。下列描述不符合以上原则的是
A. 煅烧硫铁矿时使用沸腾炉 B. 制盐酸时通入过量氯气使氢气反应完全
C. 制硫酸时使用热交换器 D. 氨碱法生产中循环使用氨气和二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA为阿伏加德罗常数的数值,下列说法正确的是
A. 1mol Na被完全氧化生成Na2O2,失去2NA个电子
B. 0.5mol锌粒与足量的盐酸反应产生H2为11.2L
C. 电解58.5g熔融的氯化钠,能产生23.0g金属钠、22.4L氯气(标准状况)
D. 标准状况下,22.4L氢气和氧气的混合气体,所含分子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年初,雾霾天气多次肆虐我国中东部地区。其中,汽车尾气和燃煤尾气是造成空气污染的原因之一。
I.汽车尾气净化的主要原理为:2NO(g)+2CO(g) ![]() 2CO2(g)+N2(g),正反应为放热反应。
2CO2(g)+N2(g),正反应为放热反应。
(1)下列说法正确的是_______________。
A.装有尾气净化装置的汽车排出的气体中一定不再含有NO或CO
B.提高尾气净化效率的最佳途径是研制高效催化剂
C.升高温度可使该反应的正反应速率增大、逆反应速率减小
D.单位时间内消耗NO和CO2的物质的量相等时,反应达到平衡
(2)已知增大催化剂的比表面积可提高化学反应速率。为了分别验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在线面实验设计表中,请在下表中的横线上填出合理数据:
实验编号 | t(℃) | NO初始浓度(10-3mol·L-1) | CO初始浓度(10-3mol·L-1) | 催化剂的比表面积(m2·g) |
① | 280 | 1.20 | 5.80 | 82 |
② | ______ | 1.20 | ______ | 124 |
③ | 350 | ______ | ______ | 82 |
实验①中,NO的物质的量浓度(c)随时间(t)的变化如下图所示。请在给出的坐标图中画出实验②、③中NO的物质的量浓度(c)随时间(t)的变化的曲线______,并标明各曲线的实验编号。
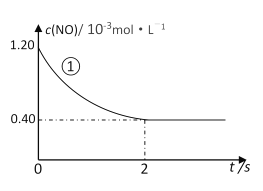
在280℃下,0~2 s内的平均反应速率v(N2) = ________________________。
II.直接排放煤燃烧产生的烟气会引起严重的环境问题。
(3)煤燃烧产生的烟气含氮的氧化物,用CH4催化还原氮氧化物(NOx)可以转化成无毒害的空气组分,从而消除氮氧化物的污染。请写出CH4催化还原NO2的化学方程式:_______________________________________________________。
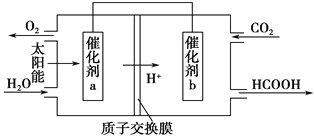
(4)将燃煤产生的二氧化碳回收利用,可达到低碳排放的目的。右上图是通过人工光合作用,以CO2和H2O为原料制备HCOOH和O2的原理示意图。催化剂a表面发生_______反应(填“氧化”或“还原”),总反应的化学方程式为________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(11分)有机物A是一种纯净的无色黏稠液体,易溶于水。为研究A的组成与结构,进行了如下实验:
实验步骤 | 解释或实验结论 |
(1)称取A物质 18.0 g,升温使其汽化,测其密度是相同条件下H2的45倍。 | 试通过计算填空: |
(2)A的核磁共振氢谱如图: | (2)A中含有_____种氢原子 |
(3)另取A 18.0 g与足量的NaHCO3粉末反应,生成0.2 mol CO2,若与足量钠反应则生成0.2 mol H2。 | (3)写出一个A分子中所含官能团的名称和数量___ |
(4)将此18.0 g A在足量纯O2中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者依次增重10.8 g和26.4 g。 | (4)A的分子式为____ |
(5)综上所述A的结构简式____ ___。 | |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】明代《天工开物》中记载:“凡铸钱每十斤,红铜居六七,倭铅(锌的古称)居三四。” 下列金属的冶炼原理与倭铅相同的是
A. Na B. Au C. Al D. Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】今有常温下两种溶液:①0.1mol/LNH3·H2O溶液②0.1mol/LNH4Cl溶液
(1)溶液①的PH______7(填“>”、“<”或“=”),写出NH3·H2O的电离方程式______________。
(2)溶液②呈________性(填“酸”、“碱”或“中”)。
(3)关于两种溶液中c(NH4+)的大小叙述正确的是________(填序号)。
A.两种溶液中c (NH4+)都等于0.lmol/L
B.两种溶液中c (NH4+)都小于0.lmol/L
C.NH4Cl溶液中c(NH4+)小于NH3·H2O溶液中c(NH4+)
(4)将溶液中①逐滴加入溶液②中,当溶液pH=7时,c(NH4+)______ c(Cl一)(填“>”、“<”或“=”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com