
| A. | 常温下,相同浓度的盐酸与氨水的混合溶液的pH=7,消耗盐酸的体积大 | |
| B. | 将pH=5的醋酸溶液稀释1000倍,溶液的pH=8 | |
| C. | 中和pH与体积均相同的盐酸和醋酸溶液,消耗NaOH的物质的量相同 | |
| D. | 常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大 |
分析 A.盐酸与氨水等物质的量反应恰好生成氯化铵,氯化铵显酸性;
B.醋酸加水稀释,促进醋酸的电离;
C.pH相同的盐酸与醋酸,醋酸的浓度大;
D.Na2S的水解程度大于NaHS.
解答 解:A.盐酸与氨水等物质的量反应恰好生成氯化铵,氯化铵显酸性,若要溶液显中性,则需要减少盐酸的量,所以消耗盐酸的体积小,故A错误;
B.醋酸加水稀释,促进醋酸的电离,溶液中氢离子的物质的量增大,所以将pH=5的醋酸溶液稀释1000倍,溶液的pH<8,故B错误;
C.pH相同的盐酸与醋酸,醋酸的浓度大于氢离子的浓度,盐酸的浓度等于氢离子的浓度,所以醋酸的浓度大于盐酸,所以中和pH与体积均相同的盐酸和醋酸溶液,醋酸消耗NaOH的物质的量大,故C错误;
D.Na2S的水解程度大于NaHS,所以常温下,同浓度的Na2S与NaHS溶液相比,Na2S溶液的pH大,故D正确.
故选D.
点评 本题考查了酸碱混合溶液定性判断及盐类水解,明确弱电解质电离特点及盐类水解特点即可解答,注意溶液中电荷守恒的应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
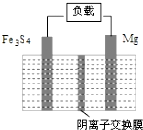 一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg$?_{充电}^{放电}$3Fe+4MgS,装置如图所示.下列说法不正确的是( )
一种高能纳米级Fe3S4和镁的二次电池,其工作原理为:Fe3S4+4Mg$?_{充电}^{放电}$3Fe+4MgS,装置如图所示.下列说法不正确的是( )| A. | 放电时,镁电极为负极 | |
| B. | 放电时,正极的电极反应式为Fe3S4+8e-=3Fe+4S2- | |
| C. | 充电时,阴极的电极反应式为MgS+2e-=Mg+S2- | |
| D. | 充电时,S2-从阴离子交换膜左侧向右侧迁移 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| X | |||
| Y | Z | W |
| A. | Z的最高价氧化物的水化物是强酸 | |
| B. | Y的最高价氧化物能溶于烧碱溶液 | |
| C. | X与W形成的化合物中含有离子键 | |
| D. | Z、W分别形成的简单离子中,前者的半径较大 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年重庆市高一上10月月考化学试卷(解析版) 题型:选择题
如何减少温室气体CO2的含量是科学家一直在探究的课题,最近中国科学技术大学的专家找到一种新型催化剂,可将CO2转化为液体燃料甲酸(CH2O2),下列说法中,不正确的是
A.地球上CO2含量上升的主要原因是植物的呼吸作用
B.CO2能吸收地面辐射,对地球有保温作用
C.CO2转化为甲酸的过程属于化学变化
D.这种新型催化剂在反应前后质量不变
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A.天然气燃烧 | B.自然界中丁达尔效应 | C.蛋白质受热凝固 | D.食醋除水垢 |
 |  |  |  |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe3O4 | B. | Fe4O5 | C. | Fe5O7 | D. | Fe7O10 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com