
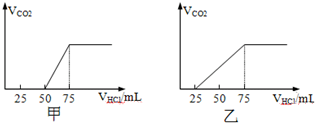
 取物质的量浓度相等的NaOH溶液两份甲和乙,每份50mL,分别向甲、乙中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的HCl溶液,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,试回答下列问题:
取物质的量浓度相等的NaOH溶液两份甲和乙,每份50mL,分别向甲、乙中通入不等量的CO2,再继续向两溶液中逐滴加入0.1mol/L的HCl溶液,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,试回答下列问题:

科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.56L |
| B、1.12L |
| C、2.24L |
| D、3.36L |
查看答案和解析>>
科目:高中化学 来源: 题型:
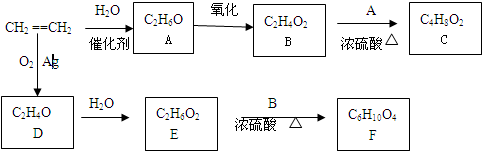
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
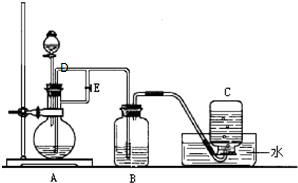 如图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化.实验时必须使用铁屑、6mol/L硫酸溶液,其他试剂任选.填写下列空白:
如图所示装置可用来制取Fe(OH)2和观察Fe(OH)2在空气中被氧化时的颜色变化.实验时必须使用铁屑、6mol/L硫酸溶液,其他试剂任选.填写下列空白:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1:1 | B、3:1 |
| C、3:2 | D、1:3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
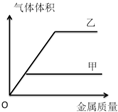 某种金属分别与等体积的甲、乙两种溶液反应所加金属的质量与相同条件下产生气体的体积关系如图所示,下列推论可能正确的是( )
某种金属分别与等体积的甲、乙两种溶液反应所加金属的质量与相同条件下产生气体的体积关系如图所示,下列推论可能正确的是( )| A、金属是镁,甲为0.2 mol/L盐酸,乙为0.1 mol/L盐酸 |
| B、金属是铁,甲为0.1mol/L稀H2SO4溶液,乙为0.1mol/L的盐酸 |
| C、金属是铝,甲为0.1 mol/L盐酸,乙为0.1 mol/L氢氧化钠溶液 |
| D、金属是铝,甲为0.1 mol/L氢氧化钠溶液,乙为0.1 mol/L盐酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 3 |
| 4 |
| A、C2H4 |
| B、C2H4O |
| C、C2H4O2 |
| D、C2H6O |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com