
| A. | ③④⑤ | B. | ②③④ | C. | ②③⑤ | D. | ①②⑤ |
分析 节能减排是指节约能源,减少二氧化碳的排放.特别是减少化石燃料的利用,是减少二氧化碳排放的重要措施.如节约电能、减少汽油的消耗、提高煤炭的利用率等都属于节能减排的措施,据此解答.
解答 解:①节能照明灯代替传统的白炽灯,可减少煤电的使用,能减少二氧化碳的排放,故①正确;
②塑料袋难降解,能够引起白色污染,不符合节能减排理念,故②错误;
③推广使用一次性筷子,大量消耗木材和能源,不利于低碳生活,故③错误;
④推广沼气照明和供热,减少煤电的使用,有利于低碳生活,故④正确;
⑤用大排量的轿车代替公交车出行,大量消耗化石燃料,不利用低碳生活,故⑤错误;
故选:C.
点评 本题考查了化学与生活关系,明确节能减排的含义,熟悉生活中常见的环境污染及资源浪费是解题关键,题目难度不大.


 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C8H18(1)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(g);△H=-48.40kJ/mol | |
| B. | C8H18(1)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(1);△H=-5518kJ/mol | |
| C. | C8H18(1)+$\frac{25}{2}$O2(g)=8CO2(g)+9H2O(l);△;△H=+5518kJ/mol | |
| D. | 2C8H18(1)+25O2(g)=16CO2(g)+18H2O(1);△H=-11036kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | Tl+的最外层有1个电子 | B. | Tl3+的氧化性比Al3+强 | ||
| C. | Tl 能形成+3价和+1价的化合物 | D. | Tl+的还原性比Ag强 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 糖类是具有甜味的物质 | |
| B. | 糖类是具有Cn(H2O)m通式的物质 | |
| C. | 淀粉是一种白色粉末,本身没有甜味 | |
| D. | 葡萄糖是一种单糖的主要原因是含有醛基 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
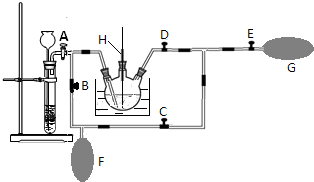
 A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应,A是常见的金属单质,D是无色气体单质、F是黄绿色气态单质,反应①②均在水溶液中进行的.
A、B、C、D、E、F六种物质的相互转化关系如图所示(反应条件未标出),其中反应①是置换反应,A是常见的金属单质,D是无色气体单质、F是黄绿色气态单质,反应①②均在水溶液中进行的.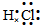 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 预期现象和结论 |
| 步骤1:取少量所得溶液于试管中,滴加3mol.L-1H2SO至溶液呈酸性,然后将所得溶液分置于A、B试管中 | |
| 步骤2: | |
| 步骤3: |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氢气和甲烷的密度都比空气的小,所以都可用向下排气法收集 | |
| B. | 配制溶质质量分数一定的溶液时,所用的烧杯必须是干燥的 | |
| C. | 蜡烛燃烧后质量变小,说明质量守恒定律不是普遍规律 | |
| D. | 通过测定两种稀盐酸的pH,可以比较它们的酸性强弱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 检验NH4+:滴入NaOH溶液后,加热,用湿润红色石蕊试纸检验发现变蓝 | |
| B. | 检验Cl-:确定溶液中无SO42-后,加入AgNO3溶液后出现白色沉淀 | |
| C. | 检验Na+:将干净的铂丝蘸取少量溶液在酒精灯上灼烧,观察火焰呈浅紫色 | |
| D. | 检验SO42-:加入BaCl2溶液出现白色沉淀,再加足量稀盐酸沉淀不溶解 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com