
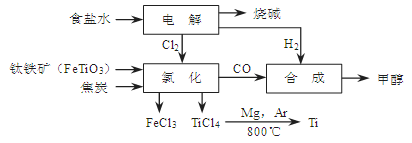
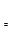 CH3OH(g)。
CH3OH(g)。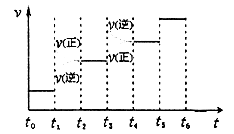
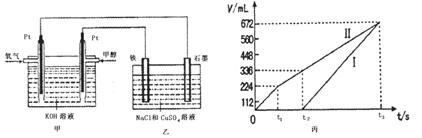
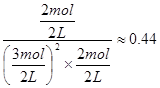 >0.27(K),说明反应向逆反应方向进行;
>0.27(K),说明反应向逆反应方向进行; CH3OH(g),正反应放热],并据图可确定“t1~t2”是加压,“t3~t4”是加热(升高温度),“t5~t6”是加催化剂;在t2~t3时间段内平衡混合物中的甲醇的含量最高。
CH3OH(g),正反应放热],并据图可确定“t1~t2”是加压,“t3~t4”是加热(升高温度),“t5~t6”是加催化剂;在t2~t3时间段内平衡混合物中的甲醇的含量最高。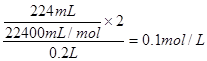 。
。

 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源:不详 题型:单选题
| A.Zn+H2SO4=ZnSO4+H2↑ | ||||
B.2KClO3
| ||||
| C.CaO+H2O═Ca(OH)2 | ||||
D.H2+Cl2
|
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.上述灼烧过程的尾气回收后可用来制硫酸 |
| B.上述过程中,由6 mol CuFeS2制取6 mol Cu时共消耗15 mol O2 |
| C.在反应2Cu2O+Cu2S===6Cu+SO2↑中,氧化产物与还原产物的物质的量比1:6 |
| D.在反应2Cu2O+Cu2S===6Cu+SO2↑中,只有Cu2O作氧化剂 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
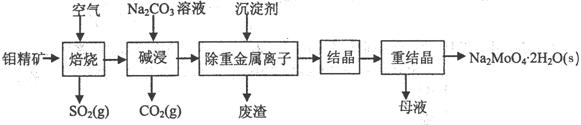 (1)焙烧的过程中采用的是“逆流焙烧”的措施,则该措施的优点是:①_______________
(1)焙烧的过程中采用的是“逆流焙烧”的措施,则该措施的优点是:①_______________
 Lix(MoS2)n。则电池放电时的正极反应式是:___________________________________。
Lix(MoS2)n。则电池放电时的正极反应式是:___________________________________。查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题



查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
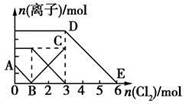
| A.线段BC代表Fe3+物质的量的变化情况 |
| B.原混合溶液中n(FeBr2)=3 mol |
| C.当通入2 mol Cl2时,溶液中已发生的离子反应可表示为: 2Fe2++2I-+2Cl2===2Fe3++I2+4Cl- |
| D.原溶液中n(Fe2+):n(I-):n(Br-)=3:1:2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:问答题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.被氧化的元素和被还原的元素的质量之比5:1 |
| B.Cl2既是氧化产物,又是还原产物 |
| C.盐酸既体现酸性,又体现酸性还原性 |
| D.转移5mol电子时,产生67.2L的Cl2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 5CO2(g)+I2(s);ΔH 1
5CO2(g)+I2(s);ΔH 1 2CO2(g);ΔH 2
2CO2(g);ΔH 2 2I2O5(s);ΔH 3
2I2O5(s);ΔH 3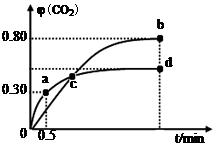
| A.容器内气体密度不变,表明反应达到平衡状态 |
| B.两种温度下,c点时体系中混合气体的平均相对分子质量相等 |
| C.增加I2O5的投料量有利于提高CO的转化率 |
| D.b点和d点的化学平衡常数:Kb<Kd |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com