

| 物质 | Fe(OH)3 | Cu(OH)2 | Ca(OH)2 | Mn(OH)2 | CuS | CaS | MnS | MnCO3 |
| pKsp | 37.4 | 19.32 | 5.26 | 12.7 | 35.2 | 5.86 | 12.6 | 10.7 |
分析 (1)高温下,Al和Mn3O4发生铝热反应生成Mn,根据反应物、生成物及反应条件书写方程式;
(2)软锰矿还原浸出得到硫酸锰溶液,说明浸取液为稀硫酸,同时溶液中还含有Ca2+、Fe3+、Cu2+等杂质,调节溶液的pH,Fe(OH)3pKap为37.4与其它离子相比最大,调节pH可以将 Fe(OH)3沉淀下来,向滤液中加入硫化铵,CuSpKap为35.2,可以将铜离子形成硫化物沉淀下来,再加入MnF2,形成CaF2沉淀,除去Ca2+,最后对得到的含有锰离子的盐电解,可以得到金属锰;
(3)锰离子和碳酸氢根离子反应生成碳酸锰沉淀、水和二氧化碳气体,根据反应物和生成物书写方程式;K=$\frac{c(CO{\;}_{3}{\;}^{2-})}{c{\;}^{2}(OH{\;}^{-})}$=$\frac{\frac{Ksp(MnC{O}_{3})}{c(Mn{\;}^{2+})}}{\frac{Ksp[Mn(OH){\;}_{2}]}{c(Mn{\;}^{2+})}}$.
解答 解:(1)高温下,Al和Mn3O4发生铝热反应生成Mn,根据反应物、生成物及反应条件书写方程式为8Al+3Mn3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Mn,
故答案为:8Al+3Mn3O4$\frac{\underline{\;高温\;}}{\;}$4Al2O3+9Mn;
(2)软锰矿还原浸出得到硫酸锰溶液,说明浸取液为稀硫酸,同时溶液中还含有Ca2+、Fe3+、Cu2+等杂质,调节溶液的pH,Fe(OH)3pKap为37.4与其它离子相比最大,调节pH可以将 Fe(OH)3沉淀下来,向滤液中加入硫化铵,CuSpKap为35.2,可以将铜离子形成硫化物沉淀下来,再加入MnF2,形成CaF2沉淀,除去Ca2+,最后对得到的含有锰离子的盐电解,可以得到金属锰,
①软锰矿还原浸出的反应为:12MnO2+C6H12O6+12H2SO4═12MnSO4+6CO2↑+18H2O,该反应中,Mn元素化合价由+4价变为+2价、C元素化合价由0价变为+4价,失电子化合价升高的反应物是还原剂,所以C6H12O6为还原剂;
反应物接触面积越大、温度越高反应速率越快,所以能提高还原浸出速率的措施:升高反应温度或将软锰矿研细等,
故答案为:C6H12O6;升高反应温度或将软锰矿研细等;
②软锰矿还原浸出的反应为:12MnO2+C6H12O6+12H2SO4=12MnSO4+6CO2↑+18H2O,溶液呈强酸性,还原浸出液中含有Mn2+、Ca2+、Fe3+、Cu2+,此时未形成沉淀,Kp为电离平衡常数,pKp=-1gKp,pKp越大,沉淀溶解平衡常数越小,滤液1为形成Fe(OH)3沉淀,pKp=-1gKp=37.4,Kp=10-37.4,Kp=c(Fe3+)×c3(OH-)=10-37.4,c(OH-)≈10-10,c(H+)=1×10-4mol/L,pH=4,所以滤液1的pH大于MnSO4浸出液的pH=4才能形成氢氧化铁沉淀,
故答案为:>;
③CaF2难溶于水,滤液2为Mn2+、Ca2+、NH4+、SO42-,加入MnF2的目的除去形成CaF2沉淀,除去Ca2+,故答案为:Ca2+;
(3)锰离子和碳酸氢根离子反应生成碳酸锰沉淀、水和二氧化碳气体,离子方程式为Mn2++2HCO3-=MnCO3↓+H2O+CO2↑;由MnCO3(s)+2OH-(aq)?Mn(OH)2(s)+CO32-(aq)可知,K=$\frac{c(CO{\;}_{3}{\;}^{2-})}{c{\;}^{2}(OH{\;}^{-})}$=$\frac{\frac{Ksp(MnC{O}_{3})}{c(Mn{\;}^{2+})}}{\frac{Ksp[Mn(OH){\;}_{2}]}{c(Mn{\;}^{2+})}}$=$\frac{10{\;}^{-10.7}}{10{\;}^{-12.7}}$=100,
故答案为:Mn2++2HCO3-=MnCO3↓+H2O+CO2↑;100.
点评 本题考查物质分离和提纯,为高频考点,涉及难溶物的溶解平衡、离子方程式书写、氧化还原反应等知识点,侧重考查基本理论,难点是难溶物溶解平衡计算,题目难度中等.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 离子半径:Cl-<Mg2+<Na+ | B. | 非金属性:Si<C<N | ||
| C. | 碱性:Mg(OH)2<NaOH<KOH | D. | 稳定性:PH3<NH3<H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
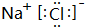 ;反应②的离子方程式为Cl2+2OH-═Cl-+ClO-+H2O;
;反应②的离子方程式为Cl2+2OH-═Cl-+ClO-+H2O;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(NH3)=0.2mol•L-1•min-1 | B. | v(NO2)=0.2mol•L-1•min-1 | ||
| C. | v(H2O)=0.005mol•L-1•s-1 | D. | v(N2)=0.005mol•L-1•s-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
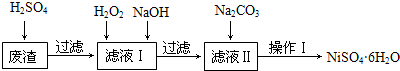
| Fe(OH)2 | Fe(OH)3 | Cr(OH)3 | Ni(OH)2 | |
| Ksp | 8.0×10-16 | 4.0×10-38 | 6.0×10-31 | 6.5×10-18 |
| 完全沉淀pH | ≥9.6 | ≥3.2 | ≥5.6 | ≥8.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化还原反应:元素化合价是否变化 | |
| B. | 共价化合物:是否含有共价键 | |
| C. | 强弱电解质:溶液的导电能力大小 | |
| D. | 氧化物:含氧化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题


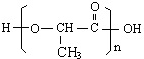
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com