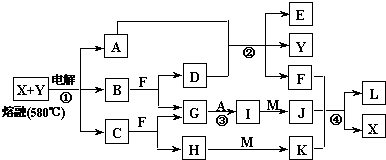
������֮���ת����ϵ��ͼ������������ʡ�ԣ�C��D����X��Y��Z������Ԫ����ɵĻ����X��Y��Z��ԭ�������������������ڱ���X��ԭ�Ӱ뾶��С��Y��Zԭ������������֮��Ϊ10��DΪ��ɫ�ǿ�ȼ�����壬GΪ����ɫ�������壬J��MΪ������I��Ư�����ã���Ӧ�ٳ���������ӡˢ��·�壮

�ݴ˻ش����и��⣺
��1��д��������A�Ļ�ѧʽ______��C�ĵ���ʽ______����������L�������ӵ��Լ���______�����Լ���ɫΪ��ɫ����
��2������E�����ڹ���______�����Լ����ƣ��õ�����ɫ������Һ�����ָ���ɫ����Ϊ��Һ�д���������______���ѧʽ����
��3��д����Ӧ�ٵ����ӷ���ʽ______��д����Ӧ�ڵĻ�ѧ����ʽ���л����ýṹ��ʽ��ʾ��______��
��4����֪F����ϡ���ᣬ��Һ�����ɫ���ų���ɫ���壬��д���÷�Ӧ�Ļ�ѧ����ʽ______��


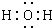
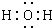


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�


 ]2-Na+
]2-Na+ ]2-Na+
]2-Na+ ��2012?����һģ����֪AΪ��ѧ��ѧ�е�һ���Σ�B��CΪ�ճ������г����Ľ�����ͨ��������D��GΪ��ɫ��ζ���壮��֪�ö��Ե缫���A��Һһ��ʱ�����ֻ��C��D��E��ϡ��Һ��������֮���ת����ϵ��ͼ�����ַ�Ӧ��������ȥ����
��2012?����һģ����֪AΪ��ѧ��ѧ�е�һ���Σ�B��CΪ�ճ������г����Ľ�����ͨ��������D��GΪ��ɫ��ζ���壮��֪�ö��Ե缫���A��Һһ��ʱ�����ֻ��C��D��E��ϡ��Һ��������֮���ת����ϵ��ͼ�����ַ�Ӧ��������ȥ����
 ]2-Na+
]2-Na+ ]2-Na+
]2-Na+