
下表为元素周期表的一部分。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA |
| 一 | ① | ||||||
| 二 | ② | ③ | ④ | ⑤ | ⑥ | ||
| 三 | ⑦ | ⑧ | ⑨ | ⑩ |
(1)表中元素________的非金属性最强;元素________的金属性最强 (填写元素符号);
(2)表中元素⑦的原子结构示意图是________;
(3)表中元素⑥⑩氢化物的稳定性顺序为________>________(填写化学式,下同);
(4)表中元素⑨和⑩最高价氧化物对应水化物的酸性:________>________;
(5) 表中元素最高价氧化物对应水化物的碱性最强的是:________ 。
科目:高中化学 来源: 题型:
如图是Zn和Cu形成的原电池,某实验兴趣小组做完实验后,记录如下:
 ①Zn为正极,Cu为负极。②H+向负极移动。③电子流动方向,从Zn经外电路流向Cu。④Cu极上有H2产生。⑤若有1 mol电子流过导线,则产生H2为0.5 mol⑥正极的电极反应式为:Zn-2e-===Zn2+描述合理的是( )
①Zn为正极,Cu为负极。②H+向负极移动。③电子流动方向,从Zn经外电路流向Cu。④Cu极上有H2产生。⑤若有1 mol电子流过导线,则产生H2为0.5 mol⑥正极的电极反应式为:Zn-2e-===Zn2+描述合理的是( )
A.①②③ B.③④⑤
C.④⑤⑥ D.②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下的密闭容器中,可逆反应2A(g) B(g)+3C(g)在下列四种状态中处于平衡状态的是( )
B(g)+3C(g)在下列四种状态中处于平衡状态的是( )
| 速率 | A | B | C | D |
| v正/mol/(L·min) | v(A)=2 | v(A)=1 | v(A)=1 | v(A)=2 |
| v逆/mol/(L·min) | v(B)=2 | v(B)=1.5 | v(C)=2 | v(A)=2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A、元素处于最高价态时一定有强氧化性;同理元素处于最低价态时一定具有强还原性。
B、将FeCl2溶液与稀HNO3混合离子反应方程式:Fe2++4H++NO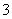 ===Fe3++NO↑+2H2O
===Fe3++NO↑+2H2O
C、HF、Al(OH)3、氨水都是弱电解质
D、颜色反应、显色反应、指示剂变色反应均属化学变化
查看答案和解析>>
科目:高中化学 来源: 题型:
(NH4)2SO4在一定条件下发生如下反应: 4(NH4)2SO4 =N2↑+6NH3↑+3SO2↑+SO3↑+7H2O
将反应后的混合气体通入BaCl2溶液,产生的沉淀为( )
A.BaSO4 B.BaSO3 C.BaS D.BaSO4和BaSO3
查看答案和解析>>
科目:高中化学 来源: 题型:
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。某同学通过如下实验探究 反应原理并验证产物。
反应原理并验证产物。
实验I:用砂纸擦去镁条表面氧化膜,将其放入盛适量滴有酚酞的饱和碳酸氢钠溶液的烧杯中,迅速反应,产生大量气泡和白色不溶物,溶液的浅红色加深。
(1)该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为
猜测2:白色不溶物可能为MgCO3
猜测3:白色不溶物可能为碱式碳酸镁[yMg(OH )2•xMgCO3]
)2•xMgCO3]
(2)为了确定产物,进行以下定性实验:
| 实验序号 | 实 验 | 实验现象 | 结 论 |
| 实验Ⅱ | 将实验I中收集到的气体点燃 | 安静燃烧, 火焰呈淡蓝色 | 气体成分为 ① |
| 实验Ⅲ | 将实验I中的白色不溶物滤出、洗涤,取少量加入足量 ② |
③ | 白色不溶物中含有MgCO3 |
| 实验Ⅳ | 取实验Ⅲ中的滤液,向其中加入适 量 ④ 稀溶液 | 产生白色沉淀,溶液红色变浅 | 溶液中存在CO32- 离子 |
实验Ⅲ中洗涤的操作方法是  。
。
(3)为进一步确定实验I的白色不溶物的成分,进行以下定量实验,装置如图所示:

称取干燥、纯净的 白色不溶物 4.52 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验后装置A增重0.36 g,装置B增重1.76 g。
白色不溶物 4.52 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验后装置A增重0.36 g,装置B增重1.76 g。
装置C的作用是 ;
白色不溶物的化学式为 。
(4)写出镁与饱和碳酸氢钠溶液反应的化学方程式 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com