
| 元素 | 相关信息 |
| X | X原子的价电子构型为nsnnpn-1 |
| Y | Y的电负性在元素周期表中最强 |
| W | W的单质是人们将太阳能转换为电能的常用材料 |
| M | M原子的最外层有两个运动状态不同的电子 |
| N | N元素基态原子的M层全充满,N层没有成对电子,只有一个未成对电子 |
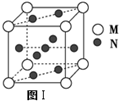 ,则该合金中M和N的原子个数比为
,则该合金中M和N的原子个数比为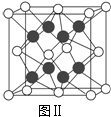 ,其中M离子的配位数是
,其中M离子的配位数是| 1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |
| 1 |
| 8 |
| 1 |
| 2 |


科目:高中化学 来源: 题型:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g?cm-3 |
| 乙醇 | -144 | 78.0 | 0.789 |
| 乙酸 | 16.6 | 118 | 1.05 |
| 乙酸乙酯 | -83.6 | 77.5 | 0,900 |
| 浓硫酸(98%) | - | 338 | 1.84 |
查看答案和解析>>
科目:高中化学 来源: 题型:
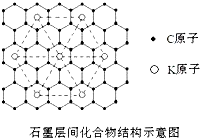 铁合金中常含有碳,铁、碳材料在日常生活、工业生产和科学研究中具有极其重要的用途.回答以下问题:
铁合金中常含有碳,铁、碳材料在日常生活、工业生产和科学研究中具有极其重要的用途.回答以下问题:
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
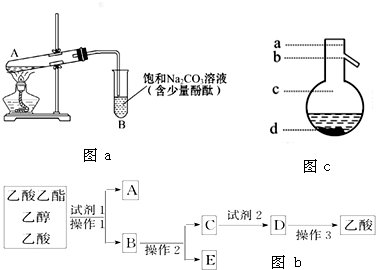
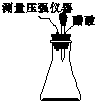 某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图所示).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.
某研究小组为探究弱酸性条件下铁发生电化学腐蚀类型的影响因素,将混合均匀的新制铁粉和炭粉置于锥形瓶底部,塞上瓶塞(如图所示).从胶头滴管中滴入几滴醋酸溶液,同时测量容器中的压强变化.| 编号 | 实验目的 | 炭粉/g | 铁粉/g | 醋酸/% |
| ① | 为以下实验作参照 | 0.5 | 2.0 | 90.0 |
| ② | 醋酸浓度的影响 | 0.5 | 36.0 | |
| ③ | 0.2 | 2.0 | 90.0 |
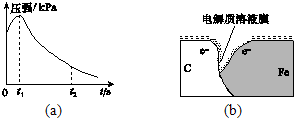 (3)该小组对图(a)中0~t1时压强变大的原因提出了如下假设,请你完成假设二:
(3)该小组对图(a)中0~t1时压强变大的原因提出了如下假设,请你完成假设二:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶解、过滤、蒸发、洗涤 |
| B、溶解、过滤、洗涤、干燥 |
| C、溶解、蒸发、洗涤、过滤 |
| D、溶解、洗涤、过滤、干燥 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com