
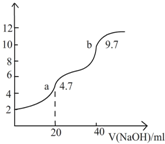
 用0.1000mol/LNaOH溶液滴定20.00mlH2A溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图所示.下列有关说法错误的是( )
用0.1000mol/LNaOH溶液滴定20.00mlH2A溶液,实验测得溶液pH随NaOH溶液体积变化曲线如图所示.下列有关说法错误的是( )| A、H2A的物质的量浓度为0.1000mol.L-1 |
| B、H2A是二元弱酸 |
| C、a-b段发生反应HA-+OH-=H2O+A2- |
| D、a点时HA-的水解程度大于电解程度 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 3 |
| 2 |

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
A、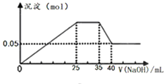 表示向含Mg2+、Al3+、NH4+的盐溶液中滴加NaOH溶液时,沉淀的量与NaOH的体积的关系图.则三种离子的物质的量之比为:n(Mg2+):n(Al3+):n( NH4+)=2:1:2,其中使用的NaOH的浓度为2mol?L-1. |
B、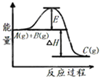 中曲线表示某反应过程的能量变化,当物质A(g)与B(g)反应生成物质C(g)时,△H>0,若使用正催化剂,E值会减小. |
C、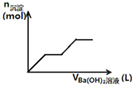 可用来表示向盐酸酸化的MgSO4溶液中加入Ba(OH)2溶液时,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)之间的关系图 |
D、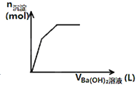 表示向一定质量的明矾溶液中滴加Ba(OH)2溶液时,产生沉淀的物质的量(n)与加入Ba(OH)2溶液体积(V)之间的关系图 |
查看答案和解析>>
科目:高中化学 来源: 题型:
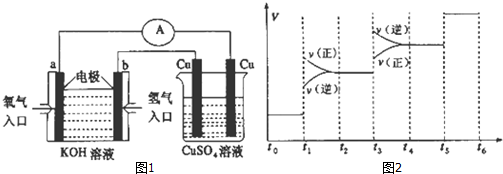
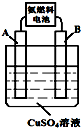 以氨气代替氢气研发氨燃料电池是当前科研的一个热点.
以氨气代替氢气研发氨燃料电池是当前科研的一个热点.
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
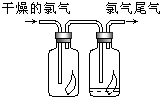 (1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是
(1)如图所示,将氯气依次通过盛有干燥有色布条的广口瓶和盛有潮湿有色布条的广口瓶,可观察到的现象是查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2SO4、Na2CO3、CaCl2 |
| B、HCl、NaOH、CuSO4 |
| C、H2CO3、CaO、Na2SO4 |
| D、HNO3、Ca(OH)2、NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、元素周期律是指元素的性质随着元素相对原子质量的递增而呈周期性变化的规律 |
| B、改变影响化学平衡的一个因素,平衡将向着抵消这种改变的方向移动 |
| C、酸碱质子理论提出凡是能给出质子的物质都是酸,能接受质子的物质都是碱 |
| D、将NH3通入CO2的NaCl饱和溶液中,可生成溶解度较小的NaHCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com