
【题目】若NA表示阿伏加德罗常数,下列说法正确的是( )
A. 相同质量的SO2和SO3所含硫原子的个数比为1:1
B. 常温下,2.7 g铝与足量的盐酸反应,失去的电子数为0.3NA
C. 0.5 mol O3与11.2 L O2所含的分子数一定相等
D. 将49 g H2SO4溶于1 L水中,所得溶液的物质的量浓度为0.5 molL-1
科目:高中化学 来源: 题型:
【题目】二茂铁是一种具有芳香族性质的有机过渡金属化合物。二茂铁熔点是173℃,在100℃时开始升华,沸点是249℃,不溶于水,易溶于苯、乙醚、汽油、柴油等有机溶剂;化学性质稳定,400℃以内不分解。实验室制备二茂铁装置示意图如下图,实验步骤为:
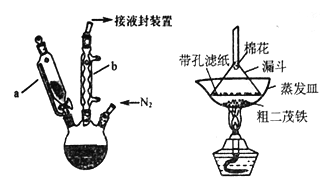
①在三颈烧瓶中加入25g粉末状的KOH,并从仪器a 中加入60mL 无水乙醚到三颈烧瓶中,充分搅拌,同时通氮气约10min;
②再从仪器a 滴入5.5 mL 新蒸馏的环戊二烯(C5H6、密度0.95g/cm3),搅拌;
③将6.5g 无水FeCl2 与(CH3)2SO(二甲亚砜,作溶剂)配成的溶液25ml 装入仪器a中,慢慢滴入三颈烧瓶中,45min 滴完,继续搅拌45min;
④再从仪器a 加入25mL 无水乙醚搅拌;
⑤将三颈烧瓶中液体转入分液漏斗,依次用盐酸、水各洗涤两次,分液得橙黄色溶液;
⑥蒸发橙黄色溶液,得二茂铁粗产品。
回答下列问题:
(1)仪器b 的名称是__________________,作用是_____________________。
(2)步骤①中通入氮气的目的是_____________________。
(3)三颈烧瓶的适宜容积应为__________ (填序号);①100ml、②250ml、③500ml;步骤⑤所得的橙黄色溶液的溶剂是_____________________。
(4)KOH、FeCl2、C5H 6反应生成二茂铁[Fe(C5H5)2]和KCl 的化学方程式为_____________________。
(5)二茂铁粗产品的提纯过程在上图中进行,其操作名称为________________。二茂铁及其衍生物可做抗震剂用于制无铅汽油,它们比曾经使用过的四乙基铅安全得多,其中一个重要的原因是_________________________________。
(6)最终得到纯净的二茂铁4.8g,则该实验的产率为___________________(保留两位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国新修订的《环境保护法》,使环境保护有了更严格的法律依据.
①为减少煤燃烧时二氧化硫的排放,对煤炭进行处理(填专有名词),同时对燃煤的烟气进行处理(填专有名词),防止造成雾霾天气.
②含铬元素的废水必须治理达标.某兴趣小组处理含Cr2O72﹣的废水的方法是用(NH4)2Fe(SO4)2将其还原为Cr3+ , 再用氨水将Cr3+转变成难溶的Cr(OH)3 . 写出用氨水将Cr3+转变成难溶的Cr(OH)3的离子方程式:;该方案处理后的废水中因含有大量元素,导致水体富营养化.
③将CO2和H2按物质的量1:4混合,在适当条件下反应可获得CH4 . 写出该反应的化学方程式: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验探究工业制乙烯的原理和乙烯的主要化学性质,实验装置如图所示(已知烃类都不与碱反应)。请回答下列问题:

(1)工业制乙烯的实验原理是烷烃(液态)在催化剂和加热条件下发生反应生成不饱和烃。例如,石油分馏产物之一的十六烷烃发生反应:C16H34![]() C8H18+甲,甲
C8H18+甲,甲![]() 4乙,则甲的分子式为________,乙的结构简式为____________________________________。
4乙,则甲的分子式为________,乙的结构简式为____________________________________。
(2)B装置中的实验现象可能是________,写出反应的化学方程式:__________,其反应类型是________。
(3)C装置中可观察到的现象是____________,反应类型是________。
(4)查阅资料知,乙烯与酸性高锰酸钾溶液反应产生二氧化碳。根据本实验中装置_____(填字母)中的实验现象可判断该资料是否真实。为了探究溴与乙烯反应是加成反应而不是取代反应,可以测定装置B中溶液在反应前后的酸碱性,简述其理由: __________________。
(5)通过上述实验探究,检验甲烷和乙烯的方法是________(选填字母,下同);除去甲烷中乙烯的方法是________。
A.气体通入水中 B.气体通过盛溴水的洗气瓶
C.气体通过盛酸性高锰酸钾溶液的洗气瓶 D.气体通过氢氧化钠溶液
(6)分别燃烧乙烯和甲烷,甲烷火焰明亮而乙烯产生少量黑烟,原因是_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2,5-已二醇C6H14O2可以作为医药中间体和制备高分子聚合物的原料。2,5-己二醇和聚酯的合成路线如下图所示:

回答下列问题:
(1)D中所含官能团的名称是____________。
(2)A→B的反应类型是________。A→D的反应条件是____________________。
(3)B→C反应的化学方程式为_____________________。
(4)G→I反应的化学方程式为___________________。
(5)物质H的同分异构体有多种,同时满足下列三个条件的共有________种,其中核磁共振氢谱为三组峰的是____________ (写结构简式)。
①能发生银镜反应;②能与碳酸氢钠溶液反应;③能发生水解反应。
(6)参照上述合成路线,以苯和乙醇为原料(试剂任选),设计制备苯乙烯的合成路线__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】请按要求回答下列问题:
(1)铝热反应在工业生产中的重要用途之一是焊接钢轨,其反应的化学方程式为:______________________;“硅材料”又被称为信息材料,作为半导体材料广泛用于制造集成电路的是____________(填化学式)。
(2)胃舒平是治疗胃酸(HCl)过多的常用药物,其中含有的有效成分是氢氧化铝,其治疗原理是(用离子方程式表示):___________________。
(3)反应2H2CrO4 + 3H2O2 = 2Cr(OH)3 + 3O2↑+ 2H2O中H2O2的变化过程为H2O2→O2。
① 该反应的还原剂是______________________________。
② 在该反应方程式中标明电子转移的方向和数目:_______________
2H2CrO4 + 3H2O2 = 2Cr(OH)3 + 3O2↑+ 2H2O
③ 若反应中转移了3 mol电子,则产生的气体在标准状况下体积为_________L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列组成生物体的化学元素中属于微量元素的一组是
A. C、H、N、P、Mn B. Cl、Fe、S、N、Mg
C. B、Cu、Zn、Mn、Mo D. N、P、K、Cu、Fe、I
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于组成生物体的化学元素,下列叙述不正确的是 ( )
A. 组成生物体的化学元素,可以分成大量元素和微量元素
B. 不同的生物体内化学元素种类和含量基本相同
C. 组成生物体的化学元素,没有一种是生物界所特有的
D. 组成玉米和人的最基本元素是碳
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com