
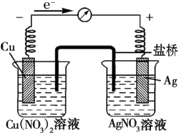
 某探究小组将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag (s)设计成原电池,某时刻的电子流向及电流表(A)指针偏转方向如图所示.
某探究小组将反应Cu(s)+2Ag+(aq)═Cu2+(aq)+2Ag (s)设计成原电池,某时刻的电子流向及电流表(A)指针偏转方向如图所示.分析 (1)Cu失电子作负极,发生氧化反应生成铜离子;
(2)电解质溶液中阳离子向正极移动,阴离子向负极移动,取出盐桥后不能形成闭合回路;
(3)Cu(NO3)2溶液中Cu电极失电子生成铜离子;
(4)根据电极方程式结合转移电子守恒计算分析.
解答 解:(1)Cu失电子作负极,发生氧化反应生成铜离子,负极的电极方程式为Cu-2e-=Cu2+;
故答案为:Cu;Cu-2e-=Cu2+;
(2)电解质溶液中阳离子向正极移动,所以盐桥中K+向正极移动,阴离子向负极移动,则NO3+向负极移动;取出盐桥后不能形成闭合回路,不能构成原电池,所以电流表的指针将不再发生偏转;
故答案为:正;负;不再发生偏转;
(3)Cu(NO3)2溶液中Cu电极失电子生成铜离子,所以Cu(NO3)2溶液中c(Cu2+)将增大;故答案为:增大;
(4)已知正极:2Ag++2e-=2Ag,负极:Cu-2e-=Cu2+,电路中转移电子的物质的量为0.5mol,则正极质量增加0.5mol×108g/mol=54g,负极质量减少$\frac{1}{2}$×0.5mol×64g/mol=16,所以两极质量差为54+16=70g;
故答案为:70.
点评 本题考查学生原电池的工作原理以及电极反应和电子转移之间的关系知识,注意把握原电池的构成条件、电极方程式的书写等基础知识的积累,题目难度不大.


 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
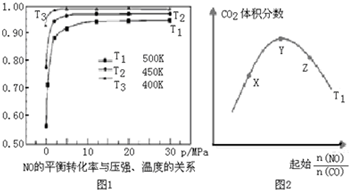
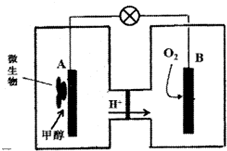 人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注.CO2和H2在一定条件下反应生成甲醇(CH3OH)等产生,工业上利用该反应合成甲醇.
人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注.CO2和H2在一定条件下反应生成甲醇(CH3OH)等产生,工业上利用该反应合成甲醇.| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol•L-1) | 0.44 | 0.6 | 0.6 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
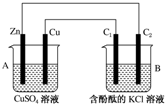 按如图所示装置进行实验,并回答下列问题:
按如图所示装置进行实验,并回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
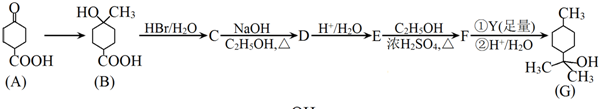
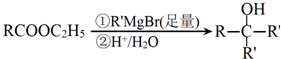
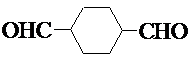 .
.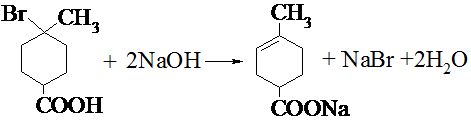 .
.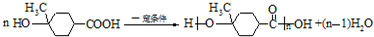 .
.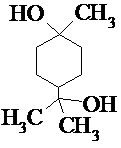 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在蔗糖中加入浓硫酸后出现发黑现象,说明浓硫酸具有脱水性 | |
| B. | 浓硝酸在光照下颜色变黄,说明浓硝酸不稳定 | |
| C. | 常温下,浓硝酸可以用铝罐贮存,说明铝与浓硝酸不反应 | |
| D. | 向碘水中滴加CCl4,振荡静置后分层,CCl4层呈紫红色,说明可用CCl4从碘水中萃取碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
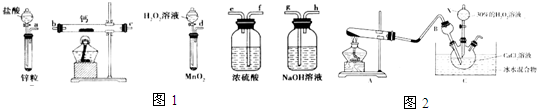
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
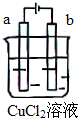
| A. | 电极a表面呈红色 | |
| B. | 电极b表面有气泡生成 | |
| C. | 电子由电源的负极沿导线流向电极b | |
| D. | 该装置能量转化形式为化学能转化为电能 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com