
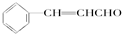 )在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如图路线合成的:
)在自然界存在于桂油中,是一种常用的植物调味油,工业上主要是按如图路线合成的: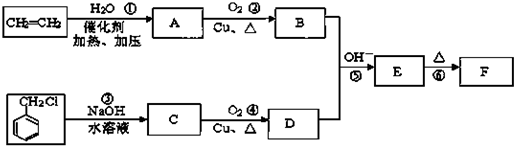
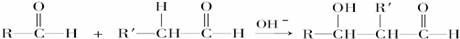
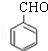 ;
;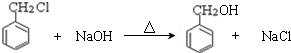 ,判断有关反应的类型:⑥消去反应;
,判断有关反应的类型:⑥消去反应;分析 CH2=CH2与水反应生成A,A为乙醇;乙醇催化氧化得到B,B为乙醛;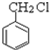 与氢氧化钠水溶液反应生成C,C为
与氢氧化钠水溶液反应生成C,C为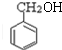 ;
; 催化氧化得到D,D为
催化氧化得到D,D为 ;乙醛和
;乙醛和 反应生成E,E为
反应生成E,E为 ;
; 发生消去反应得到F,F为
发生消去反应得到F,F为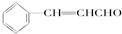 ,再结合对应有机物的结构和性质,以及前后转化关系解答该题.
,再结合对应有机物的结构和性质,以及前后转化关系解答该题.
解答 解:CH2=CH2与水反应生成A,A为乙醇;乙醇催化氧化得到B,B为乙醛; 与氢氧化钠水溶液反应生成C,C为
与氢氧化钠水溶液反应生成C,C为 ;
; 催化氧化得到D,D为
催化氧化得到D,D为 ;乙醛和
;乙醛和 反应生成E,E为
反应生成E,E为 ;
; 发生消去反应得到F,F为
发生消去反应得到F,F为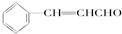 ,
,
(1)CH2=CH2与水反应生成A,A为乙醇;乙醇催化氧化得到B,B为乙醛; 与氢氧化钠水溶液反应生成C,C为
与氢氧化钠水溶液反应生成C,C为 ;
; 催化氧化得到D,D为
催化氧化得到D,D为 ,
,
故答案为: ;
;
(2)反应②中副产物为水,反应③中副产物为氯化钠,反应④中副产物为水,反应⑥中副产物为水,反应①和⑤无副产物,原子利用率100%,故答案为:①、⑤;
(3)反应③为 与氢氧化钠水溶液反应生成C,C为
与氢氧化钠水溶液反应生成C,C为 ,方程式为:
,方程式为: ;乙醛和
;乙醛和 反应生成E,E为
反应生成E,E为 ;
; 发生消去反应得到F,F为
发生消去反应得到F,F为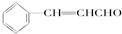 ,故反应⑥为消去反应,B为乙醛,B与新制Cu(OH)2悬浊液反应的方程式为CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O,D为
,故反应⑥为消去反应,B为乙醛,B与新制Cu(OH)2悬浊液反应的方程式为CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O,D为 ,D与银氨溶液反应的方程式为C6H5CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$C6H5COONH4+2Ag↓+3NH3+H2O,
,D与银氨溶液反应的方程式为C6H5CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$C6H5COONH4+2Ag↓+3NH3+H2O,
故答案为: ;消去反应;CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O;C6H5CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$C6H5COONH4+2Ag↓+3NH3+H2O;
;消去反应;CH3CHO+2Cu(OH)2$\stackrel{△}{→}$CH3COOH+Cu2O↓+2H2O;C6H5CHO+2Ag(NH3)2OH$\stackrel{水浴}{→}$C6H5COONH4+2Ag↓+3NH3+H2O;
(4) 的同分异构体中,苯环上有两个取代基,其中一个是羧基,则另一个是乙基,两个取代基位置关系可以为邻、间、对,故共用3种,
的同分异构体中,苯环上有两个取代基,其中一个是羧基,则另一个是乙基,两个取代基位置关系可以为邻、间、对,故共用3种,
故答案为:3;
(5)E为 ,
,
a、有醛基,能与银氨溶液反应,故a正确;
b、有羟基,能与钠反应,故b正确;
c、一个苯环能与与3个氢气反应,一个醛基能与1个氢气反应,故1mol 最多能和4mol氢气反应,故c错误;
最多能和4mol氢气反应,故c错误;
d、 中共用7种氢原子,故核磁共振氢谱中有7个峰,故d错误;
中共用7种氢原子,故核磁共振氢谱中有7个峰,故d错误;
故答案为:ab.
点评 有机推断是高考热点题型,每年高考必考,对学生的阅读和思维能力要求较高.题目信息的运用是关键.有机反应方程式的正确书写是基础.


 永乾教育寒假作业快乐假期延边人民出版社系列答案
永乾教育寒假作业快乐假期延边人民出版社系列答案科目:高中化学 来源: 题型:解答题
| ① | ② | ③ | |||
| ④ | ⑤ | ⑥ | ⑦ |
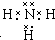 .在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所得产物不污染环境,其化学方程式是2NH3•H2O+3H2O2=N2↑+8H2O或2NH3+3H2O2=N2+6H2O.
.在微电子工业中,甲的水溶液可作刻蚀剂H2O2的清除剂,所得产物不污染环境,其化学方程式是2NH3•H2O+3H2O2=N2↑+8H2O或2NH3+3H2O2=N2+6H2O.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
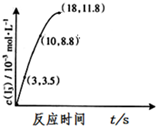 臭氧是一种强氧化剂可与碘化钾水溶液发生反应生成氧气和单质碘.向反应后的溶液中滴入酚酞,溶液变为红色.
臭氧是一种强氧化剂可与碘化钾水溶液发生反应生成氧气和单质碘.向反应后的溶液中滴入酚酞,溶液变为红色.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
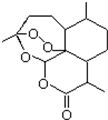 2015年诺贝尔奖获得者屠呦呦提取的抗疟新药青蒿素的结构简式,用键线式表示如图.
2015年诺贝尔奖获得者屠呦呦提取的抗疟新药青蒿素的结构简式,用键线式表示如图. ,需要在有机合成中引入羟基,引入羟基的反应类型有①②⑤.(选填编号)
,需要在有机合成中引入羟基,引入羟基的反应类型有①②⑤.(选填编号)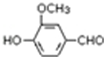 )可用于合成青蒿素,合成天然香草醛的反应如下:
)可用于合成青蒿素,合成天然香草醛的反应如下:
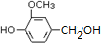 .
.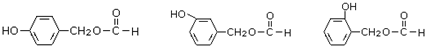 (其中之一).
(其中之一).查看答案和解析>>
科目:高中化学 来源: 题型:推断题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溶液是电中性的,胶体是带电的 | |
| B. | 直径介于1nm-100nm之间的微粒称为胶体 | |
| C. | 一束光线分别通过溶液和胶体时,后者会出现明显的光带,前者则没有 | |
| D. | 溶液中溶质分子的运动有规律,胶体中分散质粒子的运动无规律,即布朗运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 有10NA个电子转移时,放出1300kJ的能量 | |
| B. | 有1NA个水分子生成且为液体时,吸收1300kJ的能量 | |
| C. | 有2NA个碳氧共用电子对生成时,放出1300kJ的能量 | |
| D. | 有8NA个碳氧共用电子对生成时,吸收1300kJ的能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com