
| A.制农药的元素 | B.制催化剂的元素 |
| C.做半导体的元素 | D.制耐高温合金材料的元素 |
 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源:不详 题型:单选题
| A.碱性:KOH>NaOH>Mg(OH)2>Ca(OH)2 |
| B.沸点:HF<HCl<HBr<HI |
| C.热稳定性:CH4>PH3>H2O>HF |
| D.酸性:HClO4>H2SO4>H3PO4>H2SiO3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.金属性强弱:Na >Mg>Al | B.氢化物稳定性:HF > H2O >NH3 |
| C.碱性强弱:KOH>NaOH>LiOH | D.酸性强弱:HIO4 >HBrO4>HClO4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
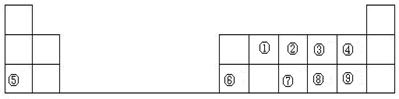
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.电子数为78 | B.质子数为53 | C.中子数为78 | D.质量数为131 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | | | | ① | | ② | ③ | |
| 3 | ⑧ | | ⑨ | ④ | | ⑤ | ⑥ | ⑦ |
| 4 | | | | | | | ⑩ | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①③ | B.②⑤ | C.①④ | D.②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
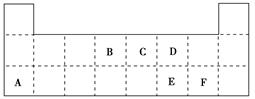
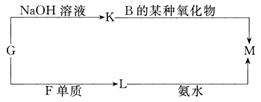
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com