
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
感光高分子也称为“光敏高分子”,是一种在激光制版及集成电路制造中应用较广的新型高分子材料。某光敏高分子A的结构简式如图所示。
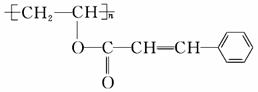
试回答下列问题:
(1)已知它是由两种单体经酯化后聚合而成的,试写出这两种单体的结构简式:________________,______________。
(2)写出由(1)中两种单体生成A的化学反应方程式:
_________________________________________________________________,
_________________________________________________________________。
(3)对高聚物A的性质判断不正确的是________。
A.在酸性条件下可以发生水解反应
B.此高聚物不能使溴水褪色
C.此高聚物可以使高锰酸钾酸性溶液褪色
D.此高聚物可与液溴发生取代反应
查看答案和解析>>
科目:高中化学 来源: 题型:
用a、b两个质量相等的Pt电极电解AlCl3和CuSO4的混合溶液[n(AlCl3):n(CuSO4)=1:9]。t1时刻a电极得到混合气体,其中Cl2在标准状况下为224 mL(忽略气体的溶解);t2时刻Cu全部在电极上析出。下列判断正确的是 ( )
A.a电极与电源的负极相连
B.t2时,两电极的质量相差3.84 g
C.电解过程中,溶液的pH不断增大
D.t2时,b的电极反应是4OH-一4e-=2H2O+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列叙述正确的是 ( )
A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+)
B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2
C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色
D.向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中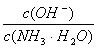 增大
增大
查看答案和解析>>
科目:高中化学 来源: 题型:
能作为氯、溴、碘元素非金属性(原子得电子能力)递变规律的判断依据的是
A.Cl2、Br2、I2的颜色 B.Cl2、Br2、I2的氧化性
C.HCl、HBr、HI的熔点 D.HCl、HBr、HI的酸性
查看答案和解析>>
科目:高中化学 来源: 题型:
关于12C18O 和14N2两种气体,下列说法正确的是
A.若体积相等,则密度相等 B.若质量相等,则质子数相等
C.若分子数相等,则体积相等 D.若原子数相等,则电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
两种气态烃以任意比例混合,在101kPa、105℃ 时1 L该混合烃与9 L氧气混合,充分燃烧后恢复到原状态,所得气体体积仍是10 L。下列各组混合烃中符合此条件的是
A.CH4 C2H4 B.CH4 C3H6 C.C2H6 C3H4 D.C2H2 C3H6
查看答案和解析>>
科目:高中化学 来源: 题型:
在元素周期表短周期元素中,A元素原子的最外层电子数是其电子层数的3倍;B元素的单质与A元素的单质化合生成化合物B2A2淡黄色固体;C元素的阳离子与A元素的阴离子电子层结构相同,0.1 mol C单质与足量盐酸反应,生成的H2在标况下体积为3.36 L;D元素与C元素同周期,D是该周期中非金属性最弱的非金属元素。
(1)各元素的符号是A________、B________、C________、D________。
(2)B元素的单质与A元素的单质化合生成化合物B2A2的化学方程式为____________________________________________。
(3)C的最高价氧化物对应水化物与NaOH溶液反应的化学方程式为________________________。
(4)D的原子结构示意图为________;气态氢化物分子式为________。
(5)物质的量相同的C和D分别与足量的强碱溶液反应生成气体的物质的量之比是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学课外小组查阅资料知:苯和液溴在有溴化铁(FeBr3)存在的条件下可发生反应生成溴苯和溴化氢,此反应为放热反应。他们设计了下图装置制取溴苯。先向分液漏斗中加入苯和液溴,再将混合液慢慢滴入反应器A中。
如图是制取溴苯的装置。试回答:

(1)装置A中发生反应的化学方程式是__________________________________。
(2)装置C中看到的现象是____________________________________,证明________________________。
(3)装置B是吸收瓶,内盛CCl4液体,实验中观察到的现象是________,原因是______________________________。如果没有B装置将A、C直接相连,你认为是否妥当?________(填“是”或“否”),理由是__________________________________________。
(4)实验完毕后将A试管中的液体倒在装有冷水的烧杯中,烧杯________(填“上”或“下”)层为溴苯,这说明溴苯________且________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com