
| A£® | ÓĆ¹żĮæ°±Ė®ĪüŹÕ¹¤ŅµĪ²ĘųÖŠµÄSO2£ŗNH3•H2O+SO2ØTNH4++SO32-+H2O | |
| B£® | MnO2ÓėÅØŃĪĖį·“Ó¦ÖĘCl2£ŗMnO2+4HCl$\frac{\underline{\;\;”÷\;\;}}{\;}$Mn2++2Cl-+Cl2”ü+2H2O | |
| C£® | ĻņFeBr2ČÜŅŗÖŠĶØČė×ćĮæĀČĘų£ŗ2Fe2++4Br-+3Cl2ØT2Fe3++2Br2+6Cl- | |
| D£® | “×Ėį³żČ„Ė®¹ø£ŗ2H++CaCO3ØTCa2++CO2”ü+H2O |
·ÖĪö A£®µēŗɲ»ŹŲŗć£»
B£®ĀČ»ÆĒāĪŖĒæµē½āÖŹ£¬Ó¦²š³ÉĄė×ÓŠĪŹ½£»
C£®ĀČĘų×ćĮ涞¼ŪĢśĄė×Ó”¢äåĄė×Ó¶¼±»Ńõ»Æ£»
D£®“×ĖįĪŖČõĖį£¬Ó¦±£Įō»ÆѧŹ½£®
½ā“š ½ā£ŗA£®ÓĆ¹żĮæ°±Ė®ĪüŹÕ¹¤ŅµĪ²ĘųÖŠµÄSO2£¬Ąė×Ó·½³ĢŹ½£ŗ2NH3•H2O+SO2ØT2NH4++SO32-+H2O£¬¹ŹA“ķĪó£»
B£®MnO2ÓėÅØŃĪĖį·“Ó¦ÖĘCl2£¬Ąė×Ó·½³ĢŹ½£ŗMnO2+4H++2Cl-$\frac{\underline{\;\;”÷\;\;}}{\;}$Mn2++Cl2”ü+2H2O£¬¹ŹB“ķĪó£»
C£®ĻņFeBr2ČÜŅŗÖŠĶØČė×ćĮæĀČĘų£¬Ąė×Ó·½³ĢŹ½£ŗ2Fe2++4Br-+3Cl2ØT2Fe3++2Br2+6Cl-£¬¹ŹCÕżČ·£»
D£®“×Ėį³żČ„Ė®¹ø£¬Ąė×Ó·½³ĢŹ½£ŗ2CH3COOH+CaCO3ØTCa2++CO2”ü+H2O+2CH3COO-£¬¹ŹD“ķĪó£»
¹ŹŃ”£ŗC£®
µćĘĄ ±¾Ģāæ¼²éĄė×Ó·½³ĢŹ½µÄŹéŠ“£¬²ąÖŲæ¼²éŃõ»Æ»¹Ō·“Ó¦Ąė×Ó·½³ĢŹ½ŹéŠ“”¢ø“·Ö½āĄė×Ó·“Ó¦·½³ĢŹ½ŹéŠ“£¬ŹģĻ¤ĪļÖŹµÄŠŌÖŹ¼°·¢Éś·“Ó¦µÄŹµÖŹŹĒ½āĢā¹Ų¼ü£¬ĢāÄæÄѶČÖŠµČ£®



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā

²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
| Ąė×Ó | Cu2+ | H+ | Cl- | SO42- |
| c/mol•L-1 | 0.5 | 2 | 2 | 0.5 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | a=1£¬b=2 | B£® | a=2£¬b=1 | C£® | a=2£¬b=2 | D£® | a=3£¬b=2 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ½ā“šĢā
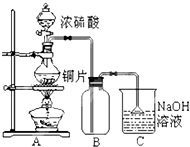 Ä³ŃŠ¾æŠŌѧĻ°Š”×éµÄĶ¬Ń§ĪŖŃéÖ¤ÅØĮņĖįÓėĶÄÜ·“Ó¦¶ųĻ”ĮņĖį²»ÄÜ£¬Éč¼ĘĮĖČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠĢ½¾æ£ŗ½«6.4g ĶʬŗĶŗ¬0.2moLČÜÖŹµÄ18.4mol/LÅØĮņĖį·ÅŌŚŌ²µ×ÉÕĘæÖŠ¹²ČČ£¬Ö±µ½ĪŽĘųĢåÉś³ÉĪŖÖ¹£®£Ø¼Ł¶ØŌŚ“Ė¹ż³ĢČÜŅŗĢå»ż²»±ä£©
Ä³ŃŠ¾æŠŌѧĻ°Š”×éµÄĶ¬Ń§ĪŖŃéÖ¤ÅØĮņĖįÓėĶÄÜ·“Ó¦¶ųĻ”ĮņĖį²»ÄÜ£¬Éč¼ĘĮĖČēĶ¼ĖłŹ¾×°ÖĆ½ųŠŠĢ½¾æ£ŗ½«6.4g ĶʬŗĶŗ¬0.2moLČÜÖŹµÄ18.4mol/LÅØĮņĖį·ÅŌŚŌ²µ×ÉÕĘæÖŠ¹²ČČ£¬Ö±µ½ĪŽĘųĢåÉś³ÉĪŖÖ¹£®£Ø¼Ł¶ØŌŚ“Ė¹ż³ĢČÜŅŗĢå»ż²»±ä£©| ŠņŗÅ | ²»ŗĻĄķµÄŌŅņ | Īó²ī £ØĘ«µĶ»ņĘ«øߣ© | øıä“ėŹ© |
| ·½°ø¢Ł | øßĆĢĖį¼ŲČÜŅŗÖŠŗ¬ÓŠĮņĖį£¬ÓėĀČ»Æ±µ·“Ó¦£¬Ź¹Éś³ÉµÄ³ĮµķŌö¶ą | Ę«µĶ | ½«ĮņĖįĖį»ÆµÄøßĆĢĖį¼ŲČÜŅŗ»»³ÉäåĖ®»ņµāĖ®»ņĻõĖįČÜŅŗ |
| ·½°ø¢Ś | ²»Ģī | ²»Ģī | ²»Ģī |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
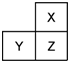 X”¢Y”¢ZŹĒČżÖÖ¶ĢÖÜĘŚµÄÖ÷×åŌŖĖŲ£¬ŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼£¬XŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒĘä“ĪĶā²ćµē×ÓŹżµÄ3±¶£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©
X”¢Y”¢ZŹĒČżÖÖ¶ĢÖÜĘŚµÄÖ÷×åŌŖĖŲ£¬ŌŚÖÜĘŚ±ķÖŠµÄĪ»ÖĆČēĶ¼£¬XŌ×ÓµÄ×īĶā²ćµē×ÓŹżŹĒĘä“ĪĶā²ćµē×ÓŹżµÄ3±¶£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø””””£©| A£® | ĘųĢ¬Ēā»ÆĪļµÄČČĪČ¶ØŠŌ£ŗX£¾Z | |
| B£® | Ō×Ó°ė¾¶£ŗX£¼Y£¼Z | |
| C£® | YŗĶZµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļ¾łĪŖĒæĖį | |
| D£® | ČōZµÄ×īøßÕż¼ŪĪŖ+m£¬ŌņXµÄ×īøßÕż¼ŪŅ²Ņ»¶ØĪŖ+m |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗŃ”ŌńĢā
| A£® | øɱł”¢ŅŗĢ¬ĀČ»ÆĒā¶¼ŹĒµē½āÖŹ | |
| B£® | Na2O”¢Fe2O3”¢Al2O3¼ČŹōÓŚ¼īŠŌŃõ»ÆĪļ£¬ÓÖŹōÓŚĄė×Ó»ÆŗĻĪļ | |
| C£® | ÓŠµ„ÖŹ²Ī¼Ó»ņÉś³ÉµÄ·“Ó¦²»Ņ»¶ØŹōÓŚŃõ»Æ»¹Ō·“Ó¦ | |
| D£® | øł¾ŻŹĒ·ń¾ßÓŠ¶”“ļ¶ūŠ§Ó¦£¬½«·ÖÉ¢Ļµ·ÖĪŖČÜŅŗ”¢×ĒŅŗŗĶ½ŗĢå |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com